血管生成(从已有的毛细血管形成新的血管)

VLoG
次浏览
更新时间:2023-05-22
血管生成
从已有的毛细血管形成新的血管
血管生成(Angiogenesis)是指从已有的毛细血管或毛细血管后静脉发展而形成新的血管,主要包括:激活期血管基底膜降解;血管内皮细胞的激活、增殖、迁移;重建形成新的血管和血管网,是一个涉及多种细胞的多种分子的复杂过程。血管形成是促血管形成因子和抑制因子协调作用的复杂过程,正常情况下二者处于平衡状态,一旦此平衡打破就会激活血管系统,使血管生成过度或抑制血管系统使血管退化。
基本信息
| 中文名 | 血管生成 |
| 外文名 | Angiogenesis |
| 含义 | 从已有的毛细血管形成新的血管 |
| 防止方法 | 丁酰甘油、透明质酸代谢物 |
| 包括 | 激活期血管基底膜降解 |
介绍
简要阐述
血管生成(Angiogenesis)是指源于已存在的毛细血管和毛细血管后微静脉的新的毛细血管性血管的生长。由于肿瘤组织这种新生血管结构及功能异常,且血管基质不完善,这种微血管容易发生渗漏,因此肿瘤细胞不需经过复杂的侵袭过程而直接穿透到血管内进入血流并在远隔部位形成转移。越来越多的研究表明,良性肿瘤血管生成稀少,血管生长缓慢;而大多数恶性肿瘤的血管生成密集且生长迅速。因此,血管生成在肿瘤的发展转移过程中起到重要作用,抑制这一过程将能明显阻止肿瘤组织的发展和扩散转移。
生成过程
生长因子

巨噬细胞
巨噬细胞
粘附因子
血管生成过程中需要血管内皮细胞(EC)与细胞外基质间、EC与EC间及EC与其他周围细胞间的相互作用。这种作用是粘附因子完成的,其中基质金属蛋白酶(MMP)通过降解基底膜糖蛋白及细胞外基质成分,启动了内皮细胞的激活和迁移,整合素家族通过和不同配基结合,介导血管内皮细胞的迁移和黏附,有助于新生血管的成熟和稳定,细胞黏附因子(ICAM-1)可产生免疫抑制和降低自然杀伤细胞的杀细胞毒性,有助于异位组织逃避机体免疫系统和自然杀伤细胞的的杀伤,促进异位组织侵入后的血管生成。
其他情况
血管生成机制复杂,参与并促进血管生成的因子也众多,EMT腹腔液中巨噬细胞数量明显增加,其分泌的TNF-α和IL-8可以促进血管内皮细胞的增殖,转化生长因子-β(TGF-β),血小板衍生内皮细胞生长因子(PD-ECGF),乙酰肝素酶,血管生成素(angs),骨生成素(OPN),环氧化酶(COX-2),缺氧诱导因子-1,层粘连蛋白(LN),胎盘生长因子(PLGF),Survivin,促红细胞生成素(Epo)均参与了EMT血管形成过程。
抑制因子类型
内皮抑制素
(ENS)
内皮抑制素为XⅧ胶原的C末端片段,能特异性抑制内皮细胞增殖,促进凋亡;抑制VEGF和bFGF等促血管生成因子和生物学作用,并且还可与基质金属蛋白酶原及整合素ανβ3、ανβ5结合,抑制内皮细胞及巨噬细胞的迁移、黏附。具有强烈的抑制新生血管形成的能力,是目前已知最强的内源性血管形成抑制因子,在肿瘤血管形成调控中发挥重要作用。
肿瘤血管
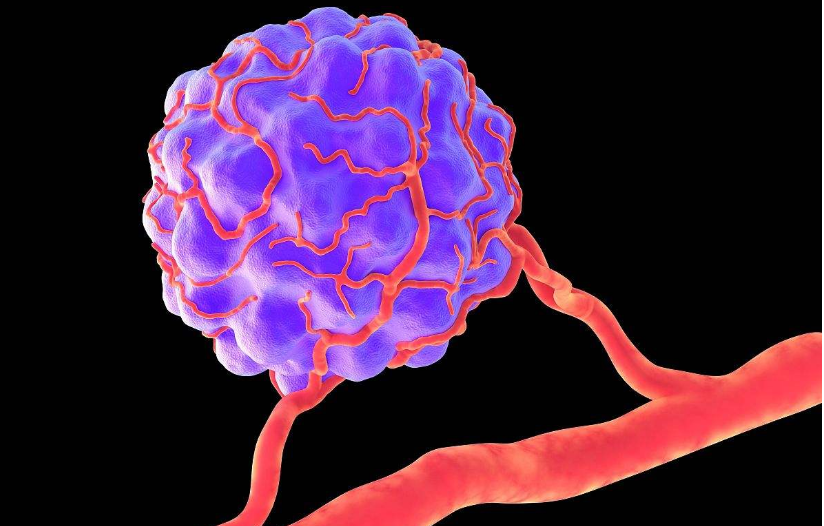
肿瘤血管
肿瘤血管
研究证实有多种活性物质可调节肿瘤血管生成,这些促进新血管生成的血管生成因子主要是一大类生长因子或细胞因子类的多肽物质如成纤维细胞生长因子(fibroblast growth factors,FGFs)、血管生成营养素、IL-1、IL-8,以及一些小分子的脂类、核苷酸及维生素,其中VEGF在血管的发生中起着重要的作用,它作为一种内皮细胞的有丝分裂原和促血管生成因子,在原位肿瘤的形成和生长以及在转移瘤的形成中起着十分重要的作用。由于VEGF能促进内皮细胞增殖、提高血管通透性以及促进内皮细胞表达PA、PAI、间质胶原酶及凝血酶活性,使血浆纤维蛋白外渗,导致纤维素在肿瘤间质中沉积,促进巨噬细胞、纤维母细胞及内皮细胞生长,从而导致肿瘤血管生成并在肿瘤生长中起重要作用。肿瘤细胞分泌的VEGF多集中在肿瘤血管周围,肿瘤血管对VEGF的反应高于正常血管,表明VEGF与肿瘤血管生成关系密切。在细胞转染实验中,经VEGF基因转染的Me157人黑色素瘤细胞可分泌大量的VEGF,裸鼠皮下接种后,肿瘤组织出现大量血管,呈放射状穿过肿瘤,提示它不仅影响肿瘤血管生成的数目,还影响血管生成的结构。
放射治疗
乏氧的肿瘤细胞,对射线的耐受能力增强:乏氧的细胞经照射后活性氧产生减少,由于射线对肿瘤细胞DNA的损伤作用主要依赖活性氧自由基,因此乏氧的肿瘤往往对射线不敏感。
放射治疗不仅对肿瘤细胞有直接或间接杀伤作用,还具有封闭肿瘤血管的作用,可使血管内皮细胞退化、变性。随着肿瘤缩小,肿瘤微血管更加迂曲、变形、管腔缩小,血流缓慢,血栓形成,使肿瘤乏氧加重。
放射治疗本身也可引起肿瘤血管生成活跃,VEGF分泌增加。


