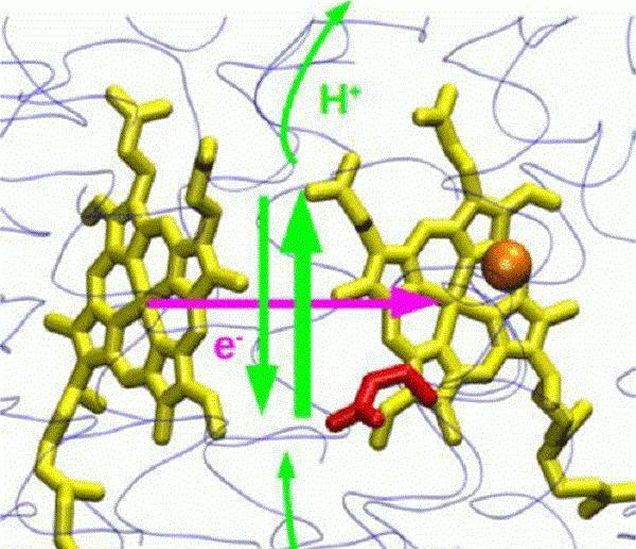
细胞色素氧化酶(电子传递链末端的酶)

VLoG
次浏览
更新时间:2023-05-23
简介
细胞色素氧化酶亦称细胞色素C氧化酶。在细胞呼吸中处于细胞色素系统的末端。此酶是把呼吸底物的电子经过细胞色素系统直接传递给分子态氧(即具有自动氧化作用)。EC1.9.3.1。通常用还原型细胞色素c的氧催化氧化的作用来进行活性测定。
凯林(D.Keilin,1930)在心肌提取物中首先发现此酶的活性。以前认为是靛酚氧化酶所催化,后来明确了靛酚反应是与细胞色素c和细胞色素c氧化酶二者都有关系。从那以后,凯林在心肌和酵母中发现与一氧化碳结合的一种细胞色素(细胞色素a3),并认为这就是细胞色素c氧化酶的原态。而且这种作用可被氢氰酸等重金属试剂强烈抑制。特别是由于一氧化碳的(对氧具有颉颃作用的)抑制作用可以为光的照射所恢复,对细胞呼吸认为与瓦勃(O.H.Warburg,1926)假设的呼吸酶为同一物质。
细胞色素氧化酶(英文名称:Cytochrome c oxidase)是一种氧化还原酶,通用名为“细胞色素-c氧化酶”,系统名称为“亚铁细胞色素-c:氧气氧化还原酶”(EC1.9.3.1)。它是一种存在于细菌或线粒体上的大型跨膜蛋白复合物。由于细胞色素氧化酶是呼吸电子传递链的第四个中心酶复合物,因此又被称为复合物IV(英文ComplexIV)。它可以接受来自四个细胞色素c的四个电子,并传递到一个氧气分子上,将氧气转化为两个水分子。在这一进程中,它结合来自基质内的四个质子来制造水分子,同时跨膜转运四个质子,从而有助于形成跨膜的质子电化学势能差,而这一势能差可以被三磷酸腺苷合酶用于制造生物体中最基本的能量分子ATP结构 细胞色素c氧化酶〔同源二聚体〕的结构,位于磷脂双分子层中。
PDB1OCC 细胞色素氧化酶复合物是一个大型蛋白质,位于粒线体内膜(inner-membrane)上,含有多个金属辅因子和13个亚基(在哺乳动物细胞中)。其中,10个亚基是来自细胞核,而另外三个亚基则是在线粒体中合成。复合物还含有两个血红素、一个细胞色素a和细胞色素a3以及两个铜中心(CuA和CuB)。实际上,细胞色素a3和CuB形成了一个双核心中心,作为氧气的还原位点。细胞色素c被呼吸链复合物III还原后,会结合到CuA双核中心,并把一个电子传递给双合中心,细胞色素c本身则恢复氧化状态(细胞色素c上的铁从+2价氧化到+3价)。被还原的CuA双核中心再将一个电子通过细胞色素a传递给细胞色素a3-CuB双核中心。在这一双核中心上的两个金属离子相距4.5Å,并通过一个处于完全氧化状态的氢氧根离子相连接。
对牛细胞色素氧化酶的结构研究显示,它发生了特殊的翻译后修饰,即其244位上的酪氨酸(Tyr244)的C6原子和240位上的组氨酸Nε原子被共价连接。这一修饰作用在细胞色素a3-CuB双核中心接受4个电子来将氧气还原为水分子的过程中发挥了重要作用。过去认为还原机制包括有一个可以导致超氧化物形成的过氧化物中间体。但普遍接受的机制是一个快速的四电子还原过程,包括迅速的氧-氧键剪切,以避免任何中间产物形成超氧化物的可能性。
应用学科
细胞生物学(一级学科);细胞生理(二级学科)
组装
生物化学性质
细胞色素氧化酶催化机制简图 细胞色素氧化酶催化的整体反应是:4Fe-细胞色素c+8H进+O2→4Fe-细胞色素c+2H2O+4H出 整个催化过程如下:首先两个电子从两个细胞色素c分子通过CuA和细胞色素a传递到细胞色素a3-CuB双核中心,将中心的金属还原为Fe和Cu。连接两个金属离子的氢氧根在被质子化后生成水分子而被释放,从而两个金属离子之间产生了一个空腔,这一空腔被一个氧气分子所填充。氧气分子与细胞色素a3中的铁原子结合形成铁氧结合形式(Fe-O2)。结合的氧很快被还原,其中一个氧原子与铁形成Fe=O形式;而另一个接近CuB的氧原子接受来自Cu的一个电子和来自Tyr244上羟基的一个电子和一个质子,被转化为一个氢氧根,同时Tyr244转变为酪氨酰自由基。来自另一个细胞色素c分子的第三个电子通过相同的途径被传递到细胞色素a3-CuB双核中心,随后这个电子和两个质子将酪氨酰自由基重新还原为酪氨酸,并将结合在CuB上的氢氧根转化为水分子。同样来自细胞色素c分子的第四个电子在进入细胞色素a3-CuB双核中心后,将Fe=O还原为Fe,同时氧原子接受一个质子转变为一个氢氧根连接于细胞色素a3-CuB中心,从而整个循环回到起始状态。整个反应过程净利用了4个还原的细胞色素c分子(提供4个电子)、4个质子(消耗8个,产生4个),将一个氧气分子还原为两个水分子。