冰盐(冰和氯化钠溶液的混合物)

VLoG
次浏览
更新时间:2023-05-23
冰盐
冰和氯化钠溶液的混合物
A点向上的线是NaCl的饱和线,一般是向右偏的,NaCl在水中溶解度随温度变化不大,这里画出一条近似竖直的线
基本信息
| 中文名 | 冰盐 |
| 外文名 | - |
| 释义 | 冰和盐溶液的混合物 |
| 类别 | |
| 性质 | 科学 |
基本介绍
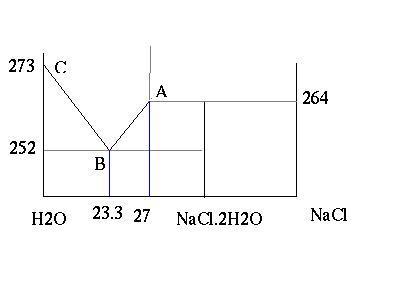
给饱和NaCl降温,在264K(-9C)析出晶体NaCl.2H2O,252K(-21C)全部变为冰和晶体NaCl.2H2O。
当给NaCl的含量23.3%的溶液降温,在252K以上都会保持液态,以下变为冰和晶体NaCl.2H2O。
AB,BC两条线是向上弯曲的,这里只是示意图,没找到数据,粗略的计算可认为是直线。
如果是给冰盐混合物升温,分析方法相同,主要是看两条水平线(温度)。
冰和NaCl混合并不能自动降低温度,只是降低了凝固点。
冰盐混合物是一种有效的驱寒剂。当盐掺在碎冰里,盐就会在冰中溶解而发生吸热作用,使冰的温度降低。冰盐混合在一起,在同一时间内会发生两种作用:一种是会大大加快冰的溶化速度,而冰溶化时又要吸收大量的热;另一种是盐的溶解也要吸收溶解热。因此,在短时间内能吸收大量的热,从而使冰盐混合物温度迅速下降,它比单纯冰的温度要低得多。
冰盐混合物的温度高低,是依据冰中掺入盐的百分数而决定的,如用盐量为冰的 23.3%时,最低温度可达-21℃。
用途
应用
常在化学实验中用来冷却或者凝固产生的低沸点物质。这一过程叫做冰盐浴。
冰盐浴的降温原理与溶液的凝固点下降有关。当食盐和冰均匀地混合在一起时,冰因吸收环境热量稍有融化 变成水,食盐遇水而溶解,使表面水形成了浓盐溶液。由于浓盐溶液的冰点较纯水低,而此时体系中为浓盐溶液和冰共存,因此体系的温度必须下降才能维持这一共 存状态(浓盐溶液和冰的共存温度应该比纯水的冰点更低)。这将导致更多的冰融化变成水来稀释浓盐溶液,在融化过程中因大量吸热而使体系温度降低。
低温冰盐浴配方:(碎冰用量100克)
浴温(℃) 盐类及用量(克) 浴温(℃) 盐类及用量(克)
-4.0 CaCl2·6H2O(20g) -30.0 NH4Cl(20g)+NaCl(40g)
-21.5 CaCl2·6H2O(81g) -30.2 NH4Cl(13g)+ NaNO3(37.5g)
-54.9 CaCl2·6H2O(143g) -37.4 NH4CNS(39.5g)+NaNO3(54.4g)
-21.3 NaCl(33g)
-17.7 NaNO3(50g) -40 NH4NO3(42g)+NaCl(42g)