氧化铝(金属铝的氧化物)

VLoG
次浏览
更新时间:2023-05-20
氧化铝
金属铝的氧化物

氧化铝(英语:Aluminium oxide/Alumina),一种无机化合物,为离子型氧化物。分子式为Al₂O₃,呈白色固体状,无臭无味,不溶于水,一般通过铝土矿(铝矾土)制得。天然的氧化铝又称刚玉,因含不同杂质而有多种颜色,如含铬元素时呈红色,称红宝石;含铁、钛元素时呈蓝色,称蓝宝石。
基本信息
中文名
氧化铝
英文名
Alumina;Aluminium oxide
别名
刚玉、三氧化二铝
CAS号
1344-28-1
性质
化学式
Al₂O₃
结构式
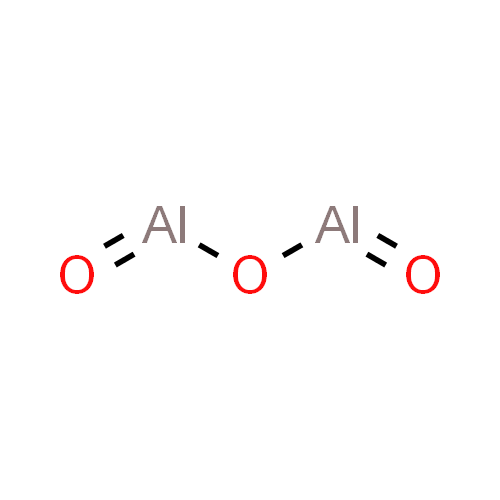
摩尔质量
101.96 g/mol
外观
白色固体
气味
无味
密度
4 g/cm³
熔点
2000℃
沸点
2980 °C
溶解性
不溶于水
危险性
NFPA 704

闪点
不可燃
氧化铝包含有多种晶型结构,包括α、β、γ、δ、ε、ζ、ŋ、θ、κ、λ、ρ-Al₂O₃等,最常见的有α-Al₂O₃、β-Al₂O₃和γ-Al₂O₃。天然刚玉为α-Al₂O₃。不同晶型的氧化铝物理化学性质不同,高温相α-Al₂O₃化学性质稳定,γ-Al₂O₃可与强酸反应生成铝盐,也能与强碱生成偏铝酸盐。
自然存在及分布
铝土矿
铝土矿是制取氧化铝的主要原料。铝土矿在全球广泛分布,且集中度高。据美国地质调查局2020年发布的矿产品摘要,世界铝土矿总资源量为550~750亿吨,在七大洲中,除南极洲外,均有铝土矿分布。其中几内亚和澳大利亚铝土矿探明储量占比巨大,在世界铝土矿格局中举足轻重。中国铝土矿储量占世界总量的3.5%。
铝土矿中含铝矿物主要包含三水铝石(Al₂O₃·3H₂O)、一水软铝石(γ-Al₂O₃·H₂O)、一水硬铝石(α-Al₂O₃·H₂O)等,同时还混杂着铁矿物(主要为赤铁矿、针铁矿等)及少量硅酸盐、钛酸盐、硫酸盐和碳酸盐等杂质。
根据矿物组成、化学成分和基底岩性特征,铝土矿可分为红土型、碳酸盐岩岩溶型,季赫温型3种类型。
天然刚玉
天然红宝石是指因含有铬元素而呈现红色的刚玉。主要产地包括缅甸、越南、泰国、柬埔寨、莫桑比克等。中国云南、新疆、吉林等地也存在部分红宝石矿床。
天然蓝宝石泛指除了红宝石以外其他颜色的刚玉,因刚玉中存在镍、钛、铁、铬等元素而呈现深蓝、浅蓝、透明、粉红、黄、绿、白等多种颜色。主要产地有泰国、斯里兰卡、马达加斯等。中国海南、福建、山东、吉林等地也发现了蓝宝石矿床。
发现及开采
1746年,德国人波特(J.H.Pott)从明矾中制得一种未知氧化物(即氧化铝)。这是第一份人工制得的氧化铝,但当时无人确定其成分。
1821年,法国地质学家贝蒂埃(Pierre Berthier)在莱博(Les Baux)小镇附近的山上发现了第一批铝土矿。于是人们根据发现地地名,将发现的矿土命名为Bauxite,中文意译为铝土矿。
1858年,法国人勒萨特里(Louis le Chatelier)提出了使用碳酸钠烧结法从铝土矿中制取氧化铝。1887年奥地利化学家拜尔(Carl Josef Bayer)成功发明了拜耳法,因其具有流程简单、作业方便,成品质量好、极佳的经济效果等特点,迅速成为工业生产氧化铝的主要手段。
氧化铝产能也随着技术发展不断提升,1894年世界第一个使用拜耳法生产氧化铝的工厂产量仅1吨/天,年产能不到400吨。到1970年,西方30%左右的工厂年产能已超过100万吨。根据国际铝业协会统计,2021年全球氧化铝产量约13858.7万吨。
晶体类型
通过对不同类型的铝土矿加工,以及采用不同加工手段,可以得到不同氧化铝晶型,如 α、β、γ、δ、ε、ζ、η、θ 型等。但不同晶型的氧化铝加热超过1200 ℃以上,都会转化为最稳定的α-Al₂O₃。所以其他晶型的氧化铝都可以看作是α-Al₂O₃的中间过渡态,被称为过渡相氧化铝。
过渡相氧化铝晶体结构的差别主要表现在原子的位置分布的变化。故过渡相之间的转化并不破坏化学键,属于位移型相变。但由过渡相转变到α-Al₂O₃的过程则是包括了原子之间的位移和化学键的重新组合,属于重组型相变,故转变不可逆。
氧化铝类型 | 晶型 | 特点 |
α-Al₂O₃ | 三方 | O²⁻近似地作六方最紧密堆积。由于这种紧密堆积的方式,使得晶体晶格能较大,所以α-Al₂O₃硬度大、熔点高,耐腐蚀性及电绝缘性好 化学性质稳定,一般不被化学试剂腐蚀(除熔融碱外) |
β-Al₂O₃ | 六方 | 为化学计量的化合物,是氧化钠和氧化铝的复合氧化物,化学式近似于Na₂O·9Al₂O₃。由4层氧离子最密填充层及松散且非固定结构的[NaO]层交替重叠构成,为层状结构 密度大、机械强度高、气孔率低具有良好的离子导电率 |
γ-Al₂O₃ | 立方 | 是氧化铝的低温亚稳形态,立方晶系,晶体为具有缺陷的尖晶石型结构 因为化合价的差异和阳离子的缺失,体积密度相对较小,固体比表面积很大,具有很高的活性、吸附性。故又称活性氧化铝,可以作吸附剂和催化剂的载体 机械性能差,高温不稳定 |
θ-Al₂O₃ | 单斜 | |
κ-Al₂O₃ | 六方 | |
ρ-Al₂O₃ | 结晶情况差,接近于无定形形态 | 活性氧化铝 |
η-Al₂O₃ | 立方 | |
λ-Al₂O₃ | 单斜 |
理化性质
物理性质
氧化铝呈白色固体状,无臭无味,不溶于水。部分天然存在的氧化铝因存在杂质而呈现不同的颜色,如含铬元素时呈红色,称红宝石;含铁、钛元素时呈蓝色,称蓝宝石。[5]氧化铝具有非常优异的机械性能,机械强度高、耐磨性好,α-Al₂O₃莫氏硬度硬度为9(最高值为10)。同时还具有优异的电绝缘性,常温电阻率为10¹² Ω·m。
以α-Al₂O₃为例,其部分物理性质数据如下。
热膨胀系数:8.5×10⁻⁶ K⁻¹
热导率:29 W(m·K)⁻¹
常温体积电阻率:10¹² Ω·m
相对介电常数:9
绝缘强度 :15kV/mm
化学性质
氧化铝是一种两性氧化物,可与强酸反应生成铝盐,也能与强碱生成偏铝酸盐。
与盐酸反应

与氢氧化钠反应

与熔融的Na₂CO₃反应

注:α-Al₂O₃常温条件下不与酸、碱发生反应。
制备方法
工业生产
拜耳法
拜耳法的原理是用NaOH溶液将铝土矿中的Al₂O₃溶解,产生铝酸钠溶液,再向溶液中加入NaOH晶种搅拌加热的条件下形成Al(OH)₃沉淀析出。主要工序包含:原矿浆制备、高压溶出、溶出矿浆的稀释、赤泥的分离和洗涤、晶种分解、水和氧化铝分级与洗涤、氢氧化铝焙烧、母液蒸发及苏打苛化等。
其主要化学过程为

拜耳法原理简单,成本及能耗低,是全球范围工业生产氧化铝使用最多的制取方法。但过程中杂质Si的析出将会带走大量的氧化铝且消耗大量碱,使得提取率降低及母液回收率降低。所以拜尔法更适合铝硅比9以上的高铝含量的铝土矿生产。
烧结法
烧结法则是在铝土矿中加入石灰石和苏打,混合后在高温下烧结得到固态的铝酸钠,再用碱溶液溶解、过滤,最后得到铝酸钠溶液。之后向铝酸钠溶液中充入二氧化碳气体,形成Al(OH)₃沉淀析出,经分离、洗涤和煅烧后获得氧化铝产品。铝土矿中的主要杂质SiO₂则是以原硅酸钙的形式进入赤土,不会带走铝土矿中的氧化铝成分,更适合高硅含量的铝土矿的生产。但烧结法工艺复杂、能耗及成本高,且生产的氧化铝质量较低。
拜尔-烧结联合法
联合法分为并联、串联和混联法三种。
并联法是拜耳法与烧结法为两个平行的生产系统,将烧结法产生的氢氧化钠溶液汇入拜耳法中,以补充拜耳法中氢氧化钠的消耗。
串联法是先用拜耳法制取大部分的氧化铝,将产生的赤泥利用烧结法进一步提取。同时将烧结法产生的铝酸钠溶液补入拜耳法系统中。
混联法则是在串联法烧结的过程中在赤泥中加入低位铝土矿,增加烧结法环节的产能。
高纯氧化铝的制备
随着新材料产业的不断发展,各领域对氧化铝的性能也有了更高的要求,需大量制备高纯、超细粒度的氧化铝。常用的制备方式包括了热解法、碳酸铝铵分解法、异丙醇盐水解法等。同时溶胶-凝胶法、化学沉淀法、激光刻蚀法、球磨法等手段也常用于实验室的少量生产,并在不断开发研究中。
常见用途
冶金领域
霍尔-埃鲁法电解氧化铝是工业制铝主要使用的方法。霍尔-艾鲁法是用直流电通入熔融的冰晶石中电解氧化铝产生金属铝。电解阳极为炭,阴极为铝液,中间态产物为氧。氧与炭阳极反应生成气态的二氧化碳,而含铝阳离子则是被还原为金属铝。其化学反应式可表示为:

机械领域
生物材料领域
氧化铝陶瓷具有生物惰性,且不可在体内降解吸收,同时具有较高的强度及耐磨性,主要用于修复或替代骨骼硬结缔组织。
氧化铝陶瓷作为植体在体内主要有形态学结合和生物学结合两种结合方式。
耐火材料
氧化铝因其耐高温、低热导等特性,被广泛应用于耐火领域,如耐火涂层、耐火砖、高温密封件、隔热板等。
电子领域
氧化铝具有较大的绝缘电阻,在电子技术领域中可以用来制造陶瓷基板、真空电容器的陶瓷管壳和半导体集成电路陶瓷封装管壳等。
光学领域
透明氧化铝陶瓷除具备普通氧化铝陶瓷的耐高温、耐腐蚀、高强度、高硬度等特性外,还具备透光、透波、激光等功能特性,可用于制作高压钠灯、金属卤灯管、透明陶瓷装甲等。
蓝、红宝石具有高光学透射率,高耐磨性、良好的光学特性,可广泛用于光学元件、传感器、光纤传感器材料、激光和衬底材料等领域。加上特有的高硬度、良好的机械性能和热稳定性,与其他材料相比,具有承受极端高温、磁场、辐射等优势,可用于极端条件。[25]世界上第一台激光器就是用红宝石作为激活介质的。
化工领域
γ-Al₂O₃、ρ-Al₂O₃等活性氧化铝具有高分散度、多孔等特点,具有很大的比表面积和孔容量,且表面呈酸性。同时具有较好的热稳定性、机械强度等优点。常被用作吸附剂、脱水剂、催化剂及催化剂载体。被广泛用于石油工业、化工、环保等领域。
电池领域
β-Al₂O₃具有良好的离子导电率。可用作钠硫(Na/S)蓄电池中的固体电解质薄膜陶瓷隔板,既可以作为离子导电体,又具有隔离钠阴极和多硫钠阳极的作用。此外β-Al₂O₃还可用于室温电池,钠-热敏元件。
环境污染
在生产氧化铝过程中产生的赤泥不仅在再利用及堆放问题上对工厂产生较大的困扰,其含碱废水会渗透到周围,污染水系和农田。
安全事宜
氧化铝虽无毒,但也会通过吸入、食入等方式对眼睛、皮肤、呼吸系统等造成刺激。
若氧化铝粉末进入眼睛,请用大量清水冲洗眼睛,并及时就医。接触氧化铝粉末时不应佩戴隐形眼镜。
若吸入大量氧化铝粉尘,请转移到干净的环境呼吸新鲜空气。


