氢离子浓度指数(溶液酸性或碱性程度的数值)

VLoG
次浏览
更新时间:2023-05-23
氢离子浓度指数
溶液酸性或碱性程度的数值

简介
pH是1909年由丹麦生物化学家SorenPeterLauritzSorensen提出。p来自德语Potenz(meanspotency,power),意思是浓度、力量,H(hydrogenion)代表氢离子(H);有时候pH
氢离子浓度指数
与其相反,如果某溶液的氢离子浓度指数为5,他的氢离子浓度为0.00001摩尔每升(mol/L),计算方法为10^(-浓度指数)
氢离子浓度指数(pH值)一般在0-14之间,在常温下(25℃时),当它为7时溶液呈中性,小于7时呈酸性,值越小,酸性越强;大于7时呈碱性,值越大,碱性越强。
当温度升高,中性对应的pH值逐渐减小【当在95℃时,中性对应的pH值=6,pH小于6时呈酸性,值越小,酸性越强;大于6时呈碱性,值越大,碱性越强。此时,氢离子浓度指数在0-12之间。
由于实际中的溶液不是理想溶液,所以仅仅用H+浓度是不可以准确测量的,因此也无法准确计算得到溶液的pH。故而应当采用H+活度,即pH=-lgaH+=-lgγ·cH+。这样从理论上讲只要知道氢离子的活度aH+就可以得到溶液的准确pH。
在常温下(25℃时),pH>7为碱性pH<7为酸性。
积常数
水的pH值
pH值是水溶液最重要的理化参数之一。凡涉及水溶液的自然现象。化学变化以及生产过程都与pH值有关,因此,在工业、农业、医学、环保和科研领域都需要测量pH值。
水的pH值是表示水中氢离子活度的负对数值,表示为:
pH=-lgaH+
pH值有时也称氢离子指数,由于氢离子活度的数值往往很小,在应用上很不方便,所以就用pH值这一概念来作为水溶液酸性、碱性的判断指标。而且,氢离子活度的负对数值能够表示出酸性、碱性的变化幅度的数量级的大小,这样应用起来就十分方便,并由此得到(在25℃下):
⑴中性水溶液,pH=7
⑵酸性水溶液,pH<7,pH值越小,表示酸性越强;
⑶碱性水溶液,pH>7,pH值越大,表示碱性越强。
溶液pH
含义

氢离子浓度指数
pH计算
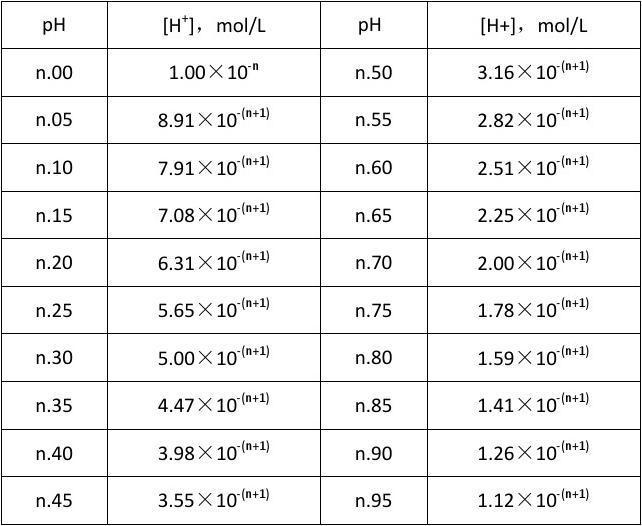
在pH的计算中[H+]指的是溶液中氢离子的物质的量浓度(有时也被写为[H3O+],水合氢离子的物质的量浓度),单位为mol/L(摩尔/升),在稀溶液中,氢离子活度约等于氢离子的浓度,可以用氢离子浓度来进行近似计算。
pH测定
有很多方法来测定溶液的pH值: 1.使用pH指示剂。在待测溶液中加入pH指示剂,不同的指示剂根据不同的pH值会变化颜色,根据指示剂的研究就可以确定pH的范围。滴定时,可以作精确的pH标准。
2.使用pH试纸。pH试纸有广泛试纸和精密试纸,用玻璃棒蘸一点待测溶液到试纸上,然后根据试纸的颜色变化对照标准比色卡可以得到溶液的pH。pH试纸不能够显示出油份的pH,原因是pH试纸以氢铁制成并以氢铁来测定待测溶液的pH值,而油中不含氢铁。
此外还有许多其他更为先进更为精确的pH值测算方法和手段。
节选自《水质PH值的测定玻璃电极法》
1适用范围
1.1本法适用于饮用水、地面水及工业废水pH值的测定。
1.2水的颜色、浊度、胶体物质、氧化剂、还原剂及高含盐量均不干扰测定;但在pH<1的强酸性溶液中,会有所谓"酸误差",可按酸度测定;在pH>10的碱性溶液中,因有大量钠离子存在,产生误差,使读数偏低,通常称为"钠差"。消除"钠差"的方法,除了使用特制的"低钠差"电极外,还可以选用与被测溶液的pH值相近似的标准缓冲溶液对仪器进行校正。
2定义
pH(X)=pH(S)+(Es—Ex)F/(RTIn10)
3原理
pOH
pOH(氢氧根离子浓度指数)是和pH相对应的表示溶液中氢氧根离子活度的概念,定义如下:
当在298K(25℃)的时候,水的离子积Kw=[H][OH]=10^(-14)因为logKw=log[H]+log[OH],所以此时pOH=14-pH。
pOH值指的是溶液的碱度,以溶液中OH-(氢氧根离子)浓度来表示,与pH所表示的溶液酸度相对应,pOH等于氢氧根离子的浓度的负常用对数,
即:pOH=-lg[OH-].
根据pOH值可以计算出溶液中氢氧根离子的浓度。
25摄氏度的水溶液中,pOH与pH值关系:
pH+pOH=14.0
所以,pH=14.0-pOH
在计算碱性溶液的pH时必须先计算出溶液的pOH,再根据pH=14.0-pOH计算出溶液的pH值。

PH测试仪
应用
准确表示溶液的pH
在标准温度(25℃)和压力下,pH=7的水溶液(如:纯水)为中性,这是因为水在标准温度和压力下自然电离出的氢离子和氢氧根离子浓度的乘积(水的离子积常数)始终是1×10⁻¹⁴,且两种离子的浓度都1×10⁻⁷mol/L。pH小说明H⁺的浓度大于OH⁻的浓度,故溶液酸性强,而pH增大则说明H⁺的浓度小于OH⁻的浓度,故溶液碱性强。所以pH愈小,溶液的酸性愈强;pH愈大,溶液的碱性也就愈强。
通常pH是一个介于0和14之间的数(浓硫酸pH约为-2),在25℃的温度下,当pH<7的时候,溶液呈酸性,当pH>7的时候,溶液呈碱性,当pH=7的时候,溶液呈中性。但在非水溶液或非标准温度和压力的条件下,pH=7可能并不代表溶液呈中性,这需要通过计算该溶剂在这种条件下的电离常数来决定pH为中性的值。
生活中的pH
pH1到2之间的是洗厕灵
pH2到3之间的是柠檬,醋
pH3是苹果
pH3到4是橘子
pH4到5是酱油
pH6是西瓜,胡萝卜
pH6到7之间的是牛奶
pH7到8之间是鸡蛋清
pH8到9之间是牙膏
pH10是肥皂
pH11是草木灰水
pH12到13之间是厨房的清洁剂
pH是水溶液最重要的理化参数之一。凡涉及水溶液的自然现象。化学变化以及生产过程都与pH有关,因此,在工业、农业、医学、环保和科研领域都需要测量pH。
来源
氢离子浓度指数(hydrogen ion concentration),一般称为“pH”,是1909年由丹麦生物化学家Soren Peter Lauritz Sorensen提出。p来自德语Potenz,意思是浓度,H(hydrogenion)代表氢离子。
计算
水的电离:水是一种极弱的电解质,可以发生微弱的电离,其电离方程式为:2H₂O≒H₃O⁺ + OH⁻,简写为H₂O≒H⁺ + OH⁻,是一个吸热的过程。水的电离受温度影响,加酸加碱都能抑制水的电离。水的电离是水分子与水分子之间的相互作用而引起的,因此极难发生。实验测得,25℃时1L纯水中只有1×10⁻⁷mol的水分子发生电离。由水分子电离出的H⁺和OH⁻数目在任何情况下总相等。25℃时,纯水中[H⁺]=[OH⁻]=1×10⁻⁷mol/L。
水的离子积常数:[H⁺]·[OH⁻]=KW,其中KW称作水的离子积常数,简称水的离子积;[H⁺]和[OH⁻]是分别是指整个溶液中氢离子和氢氧根离子的总物质的量浓度。KW只随温度变化而变化,是温度常数。如25℃,[H⁺]=[OH⁻]=1×10⁻⁷mol/L,KW=1×10⁻¹⁴;100℃时,[H⁺]=[OH⁻]=1×10⁻⁶mol/L,KW=1×10⁻¹²。
溶液酸性、中性或碱性的判断依据是:[H⁺]和[OH⁻]的浓度的相对大小.在任意温度时溶液[H⁺]>[OH⁻]时呈酸性,[H⁺]=[OH⁻]时呈中性,[H⁺]<[OH⁻]时呈碱性.但当溶液中[H⁺]、[OH⁻]较小时,直接用[H⁺]、[OH⁻]的大小关系表示溶液酸碱性强弱就显得很不方便.为了免于用氢离子浓度负幂指数进行计算的繁琐,数学上定义pH为氢离子浓度的常用对数负值,即:pH=-lg[].在pH的计算中[H⁺]指的是溶液中氢离子的物质的量浓度,单位为mol/L,在稀溶液中,氢离子活度约等于氢离子的浓度,可以用氢离子浓度来进行近似计算。
相关视频
全部
6239次播放01:45
尿常规ph值正常值
2961次播放01:16
什么是ph值?对人体有什么影响呢?
2088次播放01:22
白带PH值是什么意思?ph值偏高怎么办? 听听专家怎么说
2086次播放01:52
尿液ph值5.0是怎么回事,会不会是肾病?





