蛋白质二级结构(蛋白质多肽链有规则重复的构象)

VLoG
次浏览
更新时间:2023-05-22
蛋白质二级结构
蛋白质多肽链有规则重复的构象
基本信息
| 中文名 | 蛋白质二级结构 |
| 外文名 | secondary structure of protein |
| 定义 | 多肽链中有规则重复的构象 |
| 限于 | 主链原子的局部空间排列 |
| 结构 | α-螺旋、β-折叠、β-转角等 |
| 不包括 | 肽链其他区段的相互关系及侧链 |
收起
基本信息
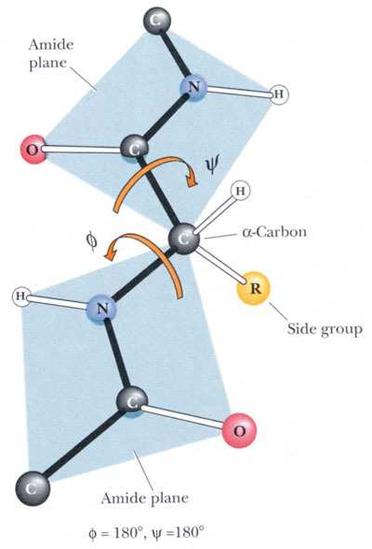
蛋白质二级结构(secondary structure of protein)指它的多肽链中有规则重复的构象,限于主链原子的局部空间排列,不包括与肽链其他区段的相互关系及侧链构象。二级结构主要有α-螺旋、β-折叠、β-转角。常见的二级结构有α-螺旋和β-折叠。二级结构是通过骨架上的羰基和酰胺基团之间形成的氢键维持的,氢键是稳定二级结构的主要作用力。
蛋白质在形成立体结构时,其多肽链部分首先折叠成α-型螺旋(Alpha Helix)和β-型(β-sheet)结构,并由此进一步可折叠成球形。此时,将α螺旋和β型结构称为二级结构。在蛋白质以外,例如在tRNA有三叶草叶型结构,也可称为二级结构。
定义:蛋白质二级结构:肽链中的主链借助氢键,有规则的卷曲折叠成沿一维方向具有周期性结构的构象。
分类
α-螺旋(α-helix)
蛋白质中常见的一种二级结构,肽链主链绕假想的中心轴盘绕成螺旋状,一般都是右手螺旋结构,螺旋是靠链内氢键维持的。每个氨基酸残基(第n个)的羰基氧与多肽链C端方向的第5个残基(第n+4个)的酰胺氮形成氢键。在典型的右手α-螺旋结构中,螺距为0.54nm,每一圈含有3.6个氨基酸残基,每个残基沿着螺旋的长轴上升0.15nm。
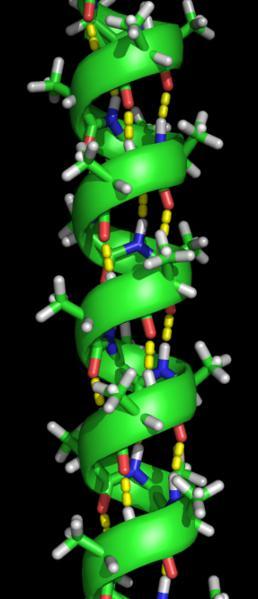
α-螺旋 黄色部分为氢键
β-折叠(β-sheet)
是蛋白质中的常见的二级结构,是由伸展的多肽链组成的。折叠片的构象是通过一个肽键的羰基氧和位于同一个肽链或相邻肽链的另一个酰胺氢之间形成的氢键维持的。氢键几乎都垂直伸展的肽链,这些肽链可以是平行排列(走向都是由N到C方向);或者是反平行排列(肽链反向排列)。
β-转角(β-turn)
多肽链中常见的二级结构,连接蛋白质分子中的二级结构(α-螺旋和β-折叠),使肽链走向改变的一种非重复多肽区,一般含有2~16个氨基酸残基。含有5个氨基酸残基以上的转角又常称之环(loops)。常见的转角含有4个氨基酸残基,有两种类型。转角I的特点是:第1个氨基酸残基羰基氧与第4个残基的酰胺氮之间形成氢键;转角II的第3个残基往往是甘氨酸。这两种转角中的第2个残基大都是脯氨酸。
无规卷曲(random coil)
此种结构为多肽链中除以上几种比较规则的构象外,其余没有确定规律性的那部分肽链的二级结构构象。
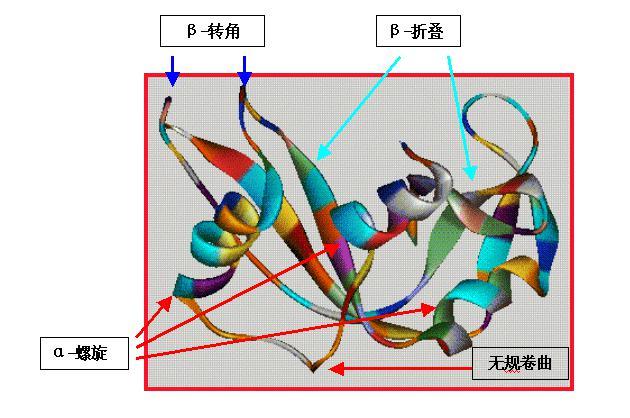
蛋白质的二级结构


