Toll样受体(1980年发现的蛋白质分子)

VLoG
次浏览
更新时间:2023-05-22
Toll样受体
1980年发现的蛋白质分子
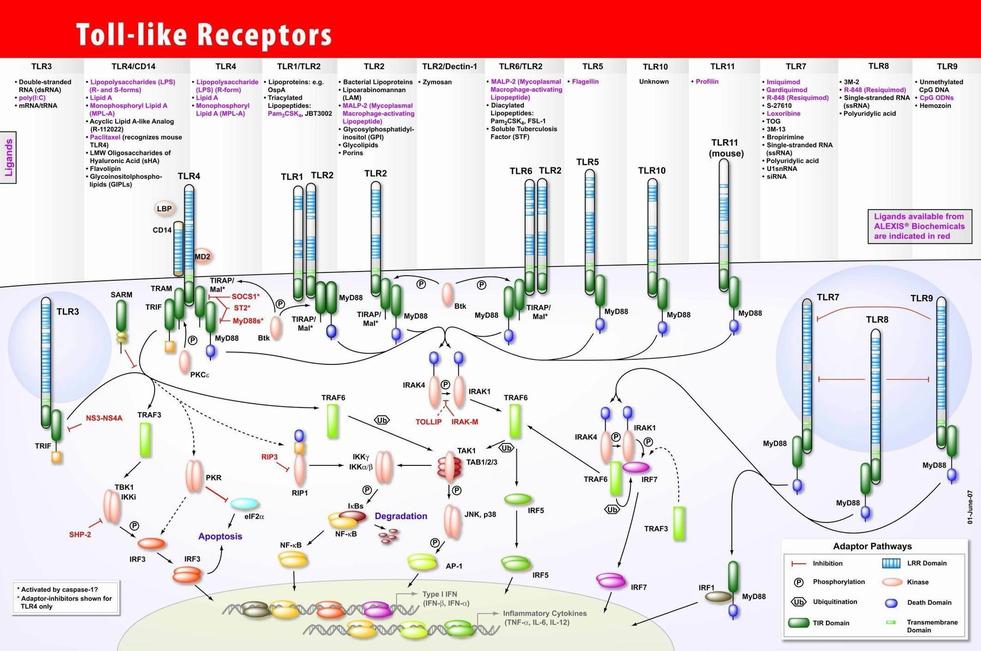
新近研究发现,TLR能结合机体自身产生的一些内源性分子(即内源性配体)。免疫佐剂可增强抗肿瘤免疫,其分子和细胞机制得到进一步阐明TLR也在其中扮演重要角色。由于肿瘤在发生发展过程中可以产生一些能被TLR识别的内源性配体,所以TLR在肿瘤免疫监视中可能发挥了一定作用。
基本信息
| 中文名 | Toll样受体 |
| 外文名 | Toll-like receptors |
| 别名 | TLR |
| 类型 | |
| 发现时间 | 1980年 |
分子概述
Toll样受体(Toll-like receptors,TLR)是参与非特异性免疫(天然免疫)的一类重要蛋白质分子,也是连接非特异性免疫和特异性免疫的桥梁。TLR是单个的跨膜非催化性蛋白质,可以识别来源于微生物的具有保守结构的分子。当微生物突破机体的物理屏障,如皮肤、粘膜等时,TLR可以识别它们并激活机体产生免疫细胞应答。
发现历史
早在19世纪人们了解到微生物致病的概念后,就想到多细胞生物体中应该存在这样的分子,它们能够识别微生物特有的分子,从而识别入侵的微生物。早在100多年前,人们就开始寻找这样的分子。德国著名细菌学家科赫的弟子理查德菲佛(Richard Pfeiffe)创造了”内毒素“一词来称呼革兰氏阴性细菌中能够造成动物发热和休克的一种成分。后来人们发现这种物质是大多数革兰氏阴性细菌产生的脂多糖(LPS)。人们又发现,另外一些分子,如细菌脂肽、鞭毛蛋白、非甲基化DNA等,能够激发宿主的保护性应答,但是如果这样的应答持续过久或者强度过大,就会造成伤害。于是人们从逻辑上推定机体中必定存在这样的分子的受体,它们可以向机体发出存在感染的警报。然而时隔多年人们却没有找到这样的受体。
1980年,Nusslein-Volhard等在研究果蝇胚胎发育过程中发现有一个基因决定着果蝇的背腹侧分化,将其命名为Toll基因。1988年,Hashimoto等人发现Toll基因编码一种跨膜蛋白质,并阐明了Toll蛋白的结构。1991年,Gay等人发现,Toll蛋白在结构上与哺乳动物中一种天然免疫功能分子——白细胞介素1受体(IL-1R)具有同源性:二者的细胞质部分相似。这第一次提示了人们Toll可能和免疫有关。1994年,Nomura等人首先报道了人中的Toll样受体。然而当时Toll的免疫学功能没有得到阐明,所以人们仍然认为Toll样受体是和哺乳动物的发育有关的。不过,两年之后的1996年,Jules A.Hoffmann和他的同事们发现Toll在果蝇对真菌感染的免疫中起着重要作用,从而确立了Toll的免疫学意义。翌年,Charles Janeway和Ruslan Medzhitov阐明了一种Toll样受体(后来被命名为TLR4)能够激活与适应性免疫有关的基因。Bruce A.Beutle随后发现TLR4能够探测LPS的存在。后来他们又发现,如果使小鼠中的TLR4突变而丧失功能,小鼠不会对LPS起反应。
后来,科学家们用基因打靶的方式使其他各种TLR丧失功能进行了研究。结果人们认为,每种TLR可识别不同的一类分子。
自此,人们不但揭示了Toll样受体在免疫学上的意义,也揭开了100多年前人们寻找的那个谜底。
受体结构
所有Toll样受体同源分子都是Ⅰ型跨膜蛋白,可分为胞膜外区,胞浆区和跨膜区三部分。
Toll样受体胞膜外区主要行使识别受体及与其他辅助受体(co-receptor)结合形成受体复合物的功能。Toll样受体的胞浆区与IL-1R家族成员胞浆区高度同源(IL-1R介导的信号传导系统和机制与果蝇类似),该区称为Toll-IL-1受体结构域(Toll-IL-1 receptor domain,TIR结构域)。TIR具有嗜同性相互作用(homophilic interaction),藉此来募集下游含有TIR的信号分子,组成信号复合体。但是二者胞外部分不相关,TLR胞膜外区为有17个~31个亮氨酸富集的重复序列(Leucine rich repeats,LRRs),并且都含有3个胞外段辅助蛋白即MD-1、MD-2和RP105,参与对疾病相关分子模式(PAMP)的识别;而IL-1R为Ig样的结构,在哺乳动物中,一些胞浆蛋白也存在TIR域,如2种信号接受蛋白,MyD88和TIR域的接受子蛋白(TIR domain-containing adaptor protein,TIRAP),二者在TIR信号传导中起作用。
受体分类
目前,在哺乳动物及人类中已经发现的人TLRs家族成员有11个。其中了解比较清楚的有TLR2,TLR4,TLR5和TLR9。人的TLRs家族基因定位分别是定(TLR1,2,3,6,10)4号染色体,9号染色体(TLR4),1号染色体(TLR5),3号染色体(TLR9),x号染色体(TLR7,8)。
根据TLRs细胞分布特征,可将其分为普遍存在型(TLR1)、限制存在型(TLR2、TLR4、TLR5)及特异存在型(TLR3)3类。
根据染色体的位置、基因结构和氨基酸序列,人的TLRs受体可以分为5个亚科,即TLR2,TLR3,TLR4,TLR5和TLR9。TLR2亚科有TLR1,TLR2,TLR6和TLR10;TLR9亚科有TLR7,TLR8和TLR9;TLR3,TLR4和TLR5各自形成一个亚科。
受体分布
受体功能
Toll样受体在天然免疫中的识别作用
●TLR4可以识别革兰氏阴性菌脂多糖(LPS),还可识别宿主坏死细胞释放的热休克蛋白(heat-shockproteins,HSP),体内类肝素硫酸盐和透明质酸盐降解的多糖部分以及局部的内源性酶的级联活化反应也可激活TLR4。
●TLR2的配体较TLR4的广泛,包括脂蛋白,脂多肽,脂肪酸(LTA)阿拉伯甘聚糖(LAM)及酵母多糖等。
●TLR3特异识别病毒复制的中间产物ds-RNA,从而激活NF-кB和干扰素IFN-β前体。DoyleS E等证实,抗TLR3单克隆抗体能抑制成纤维细胞IFN-β的产生。Christopher A等证实TLR3还具有调控鼻病毒对人支气管细胞感染的能力,这也说明了TLR3在宿主抵抗活病毒中发挥重要的作用。
●TLR7识别咪喹啉家族低分子量的咪唑莫特、R-848和R-847等。
TLR7、TLR8和TLR9高度同源,与其他TLR不同,它们在细胞内涵体中起作用,吞噬和包膜溶解后结合它们的配体,可识别微生物的核酸。
另外,TLR对配体的识别,不同类型的TLRs可以组合,从而识别不同的PAMPs,如TLR1与TLR6可以协同TLR2对不同的PMAPs分子进行组合识别;TLR7可能同TLR9组合来介导CpG激活免疫细胞。其中TLR4/TLR4和TLR9/TLR9是以同源二聚体的形式进行;而TLR2/TLR4、TLR2/TLR6和TLR7/TLR8为异源二聚体,还有的二聚体中有一个亚单位尚未确定,如TLR3/TLR、TLR5/TLR。
Toll样受体在获得性免疫系统中的作用
首先,Toll样受体在获得性免疫中的具有识别作用。机体最强的抗原呈递细胞——树突细胞可表达TLR。借助TLR识别LPS、GpG-DNA、肽聚糖、脂蛋白以及分支杆菌的细胞壁成分等具有PAMP的分子,树突细胞被活化而成熟,提供获得性免疫的共刺激信号。因此TLR是微生物成分引起树突细胞活化的桥梁。
第二,Toll样受体对获得性免疫应答类型具有调控作用。多数TLRs活化后可以诱导抗微生物防御系统,产生IL-1β、IL-6和TNF以及趋化型细胞因子,从而调节机体Th1和Th2两种方面的平衡。
具体地说,TLR3、TLR7/TLR8、TLR9在病毒核酸成份的刺激下,诱导机体产生I型干扰素,后者发挥抗病毒免疫作用。TLR2和TLR4激活DC后产生不同的细胞因子和化学激活因子。TLR4主要产生IL-12 p70,IFN-γ介导蛋白(IP-10)及转录IFN-β。TLR2刺激则优先表达IL-8和IL-23。这些可溶性细胞因子诱导T辅助细胞向有利于杀灭病原的方向分化产生细胞免疫应答或体液免疫应答。尤其是IL-12和IP-10能够刺激T细胞产生IFN,促使Th细胞分化为Th1细胞。如果缺乏IL-12则分化为Th2细胞。
另一方面,TLR2优先激活p19的转录。p19是近期才被证明的一种可以和p40形成杂二聚体的蛋白,与IL-12具有相似的作用。TLR4激动剂可刺激大量产生IP-10。IP-10是不同细胞对IFN-γ、微生物成分应答后产生的CXC化学激活因子,可对单核细胞、NK细胞产生化学吸附作用,更重要的是Th1型细胞优先表达IP-10受体CXCR3,但TLR2刺激DC不能表达IP-10。


