碘化银(碘和银的化合物)

VLoG
次浏览
更新时间:2023-07-17
小编整理:
碘化银是一种无机物,化学式为AgI,为亮黄色无臭微晶形粉末。它有α和β两种类型,其中α型为立方晶体,密度为6.010g/立方厘米,熔点为558℃,沸点为1506℃。β型为六方晶体,密度为5.683g/立方厘米,加热到146℃即转为α型。 碘化银不溶于稀酸和水,微溶于氨水,但易溶解于碘化钾、氰化钾、硫代硫酸钠和甲胺。它是一种重要的感光材料,可应用于摄影、人工降雨等领域。 总之,碘化银是一种化合物,由碘和银组成,具有特定的化学性质和用途。碘化银
碘和银的化合物

基本信息
中文名
碘化银
水溶性
难溶:3 × 10-7g/100mL (20 °C)
熔点
558 ℃
沸点
1506 ℃
密度
5.683g/cm3 (30℃)
外观
亮黄色无臭微晶形粉末
化学式
AgI
摩尔质量
234.773 g·mol−1
EINECS登录号
232-038-0
应用
CAS号
7783-96-2
英文别名
silver iodide
分子量
234.77
结构
理化性质
物理性质
外观与性状: | 亮黄色无嗅微晶形粉末, 有感光性。 | ||
熔点(℃): | 558 | 相对密度(水=1): | 5.67 |
沸点(℃): | 1506 | 相对蒸气密度(空气=1): | 无资料 |
分子式: | AgI | 分子量: | 234.77 |
主要成分: | 纯品 | ||
溶解性: | 不溶于水,不溶于氨水,溶于碘化钾等。 | ||
其它理化性质: | 552 | ||
在光的作用下,碘化银分解成极小颗粒的“银核”,而逐渐变为带绿色的灰黑色。
化学性质
α型为亮黄色六方晶体。溶于氰化钾、硫代硫酸钠、碘化钾,微溶于浓氨水。
计算化学数据
1、疏水参数计算参考值(XlogP:无
2、氢键供体数量:0
3、氢键受体数量:0
4、可旋转化学键数量:0
5、互变异构体数量:无
6、拓扑分子极性表面积:0
7、重原子数量:2
8、表面电荷:0
9、复杂度:2
10、同位素原子数量:0
11、确定原子立构中心数量:0
12、不确定原子立构中心数量:0
13、确定化学键立构中心数量:0
14、不确定化学键立构中心数量:0
15、共价键单元数量:1
安全信息
危险运输编码:暂无
危险品标志:暂无
安全标识:S22S24/25
危险标识:R36/37/38
化学信息
碘化银有α,β和γ相,在常温下β和γ相较为稳定,α相有较高的导电性,但是在低温条件下难以存在。β相为六方晶体,γ相为立方晶体。在146摄氏度以上α相会逐渐变为主导,它是体心立方晶体。
编号系统
CAS号:7783-96-2
MDL号:MFCD00003412
EINECS号:232-038-0
RTECS号:暂无
BRN号:暂无
PubChem号:24846565
毒理学数据
接触或吸入本品可对皮肤、眼睛及呼吸道造成损害。长期接触可引起局部或全身性银质沉着,发生局部或全身皮肤沉着症。工作人员应作好防护,若不慎触及,应立即用水冲洗。
制取方法
实验室制备
由硝酸银溶液逐渐加入碘化钾溶液后,过滤,再用热水洗净而制得(应在暗室或红光下进行)。
微粒的制备
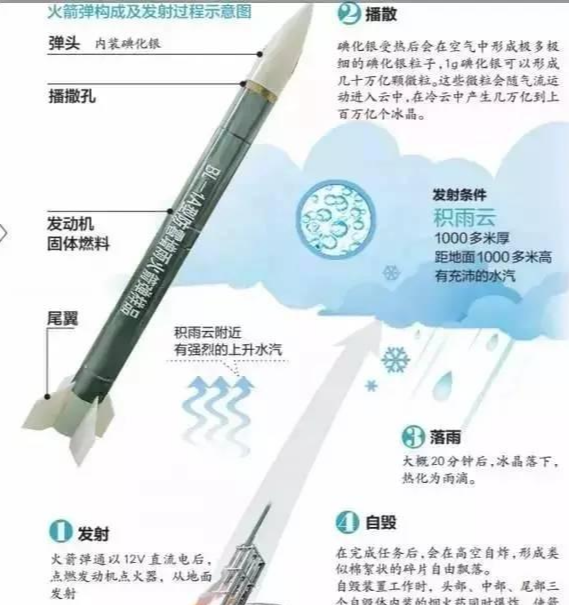
(3)碘化银炮弹。碘化银同炸药一起在弹头爆炸时形成微粒。
(4)碘化银水溶胶。用碘化钠和硝酸银配制而成。
储存
密封避光保存。贮存于阴凉、通风的库房。远离火种、热源。保持容器密封。应与氧化剂、酸类分开存放,切忌混贮。
用棕色玻璃瓶包装,瓶口用蜡密封。储存于阴凉、干燥、避光处。运输过程中重心轻放,严禁撞击、震动,以防瓶破。
用途
感光乳剂
催化剂
人工降雨
在人工降雨中的用途:冰核形成剂。碘化银催化,广泛应用于人工降水、人工防雹、人工削弱台风、人工抑制闪电以及人工消云和人工消雾等试验研究中。碘化银之所以能用于人工降雨,在于碘化银微粒结构与冰结构很相似,且每克碘化银在-10℃的气温下产生的冰核大约为1012 ~1014 个,是一种很好的人工冰核,是冷云内人工产生冰晶的一种较好的物质。碘化银在人工降雨中所起的作用在气象学上称作冷云催化。碘化银只要受热后就会在空气中形成极多极细(只有头发直径的百分之一到千分之一)的碘化银粒子,碘化银在空中分解生成银和碘单质。1g碘化银可以形成几十万亿个微粒。这些微粒会随气流运动进入云中,在冷云中产生几万亿到上百亿个冰晶,有助于降雨。除碘化银外,干冰、液氮也常常作为人工影响天气的催化剂。
其它
此外,碘化银还能防冰雹、防霜冻、防雪、防风暴,甚至可以防台风。
生产方法
复分解法:将相对密度1.1的碘化钾溶液加入反应器中,边剧烈搅拌边缓慢加入相对密度1.1~1.2的硝酸银溶液,直至碘化钾溶液过量约3%左右为止。此时生成黄色碘化银沉淀,经静置、过滤、用蒸馏水洗涤,再经离心分离,在70℃以下干燥,制得碘化银成品。其KI+AgNO3→AgI↓+KNO3以上操作应在暗室或红光下进行。过滤的母液回收,副产硝酸钾。
碘化银微粒的发生方法有:
(1)碘化银发生炉。在碘化银发生炉中燃烧碘化银丙酮溶液(加有碘化纳、碘化钾或碘化按等助溶剂),以使碘化银蒸汽在空气中冷却结晶成微粒。
(3)碘化银炮弹。碘化银同炸药一起在弹头爆炸时形成微粒。
(4)碘化银水溶胶。用碘化钠和硝酸银配制而成,通过喷撒形成微滴。不同方法产生的碘化银微粒成冰率有很大差异,碘化银发生炉和烟火剂的成冰率较高,而烟火剂和炮弹法则在单位时间内输出率较高。撒播手段一般用飞机或高炮,但碘化银发生炉和烟火筒也可在地面使用,并靠气流和扩散进入云中。根据作业对象和要求可选用不同的催化手段和发生方法,以保证在云中要求的部位产生一定数量的人工冰晶。
注意事项
危险性概述
环境危害:对环境有危害,对水体可造成污染。
燃爆危险:本品不燃。
急救措施
皮肤接触:脱去污染的衣着,用流动清水冲洗。
吸入:脱离现场至空气新鲜处。如呼吸困难,给输氧。就医。
食入:饮足量温水,催吐。就医。
消防措施
灭火方法:消防人员必须穿全身防火防毒服,在上风向灭火。灭火时尽可能将容器从火场移至空旷处。[
泄漏应急处理
操作处置与储存
操作注意事项:密闭操作,加强通风。操作人员必须经过专门培训,严格遵守操作规程。建议操作人员佩戴自吸过滤式防尘口罩,戴化学安全防护眼镜,穿防毒物渗透工作服,戴乳胶手套。避免产生粉尘。避免与氧化剂、酸类接触。搬运时要轻装轻卸,防止包装及容器损坏。禁止震动、撞击和摩擦。配备泄漏应急处理设备。倒空的容器可能残留有害物。
储存注意事项:储存于阴凉、通风的库房。远离火种、热源。保持容器密封。应与氧化剂、酸类分开存放,切忌混储。储区应备有合适的材料收容泄漏物。
个体防护
眼睛防护:戴化学安全防护眼镜。
身体防护:穿防毒物渗透工作服。
手防护:戴乳胶手套。
其他防护:工作完毕,淋浴更衣。保持良好的卫生习惯。
安全术语
Donotbreathedust.切勿吸入粉尘。
Avoidcontactwithskinandeyes.避免与皮肤和眼睛接触。
法规信息
化学危险物品安全管理条例(1987年2月17日国务院发布),化学危险物品安全管理条例实施细则(化劳发[1992]677号),工作场所安全使用化学品规定([1996]劳部发423号)等法规,针对化学危险品的安全使用、生产、储存、运输、装卸等方面均作了相应规定。
知识拓展
云是由水汽液化而成,高炮人工降雨就是将含有碘化银的炮弹打入云雾厚度比较大的4000至5000米中低高空,碘化银在高空扩散,成为云中水滴的凝聚核,水滴在其周围迅速凝聚,达到一定体积后便产生了降雨。
世界上许多国家普遍使用碘化银做人工降雨的催化剂。中国采用干冰和碘化银穿插使用的办法。干冰是由人工降雨飞机的舱底“漏斗”洒向云层。碘化银做催化剂时,可用火箭把碘化银焰弹发射上去。
人工降雨常见催化剂的应用原理
1.干冰的应用原理
干冰即固态二氧化碳。通常二氧化碳气体在加压和降温的条件下,会变成无色液体,再降低温度,即会变成雪花般的固体,经过压缩,就会成干冰。论外貌,干冰和普通的冰确实很相像,其外形与冰一样。在一个标准大气压下,受热后不会立即熔化,而是在-78.5℃时直接变成气体,销声匿迹,不像冰熔化后会留下水迹,因而得名“干冰”。
干冰汽化时使周围空气层温度下降,云层温度下降,从而引起水滴的凝结,凝结的水滴冰晶迅速加大增多,最后形成降雨。
2.碘化银的应用原理
碘化银只要受热后就会在空气中形成极多极细(只有头发直径的百分之一到千分之一)的碘化银粒子。因此,用碘化银催化降雨不需飞机,设备简单、用量很少,费用低廉,可以大面积推广。除了人工降水(雨、雪)外,碘化银还可以用于人工消云雾、消闪电、削弱台风、抑制冰雹等。


