氮化硅(重要的结构陶瓷材料)

VLoG
次浏览
更新时间:2023-05-20
氮化硅
重要的结构陶瓷材料

历史
亨利·爱丁·圣克莱尔·德维尔和弗里德里希·维勒在1857年首次报道了氮化硅的合成方法。在他们报道的合成方法中,为减少氧气的渗入而把另一个盛有硅的坩埚埋于一个装满碳的坩埚中加热。他们报道了一种他们称之为硅的氮化物的产物,但他们未能弄清它的化学成分。1879年PaulSchuetzenberger通过将硅与衬料(一种可作为坩埚衬里的糊状物,由木炭、煤块或焦炭与粘土混合得到)混合后在高炉中加热得到的产物,并把它报道为成分是Si3N4的化合物。1910年路德维希·魏斯和特奥多尔·恩格尔哈特在纯的氮气下加热硅单质得到了Si3N4。1925年Friederich和Sittig利用碳热还原法在氮气气氛下将二氧化硅和碳加热至1250-1300℃合成氮化硅。
晶体结构和特性
蓝色圆球是氮原子,灰色圆球是硅原子
氮化硅(Si3N4)存在有3种结晶结构,分别是α、β和γ三相。α和β两相是Si3N4最常出现的型式,且可以在常压下制备。γ相只有在高压及高温下,才能合成得到,它的硬度可达到35GPa。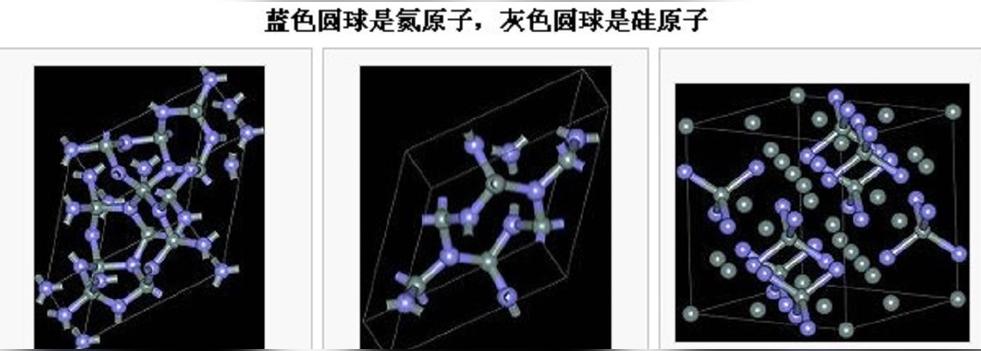

氮化硅
合成方法
六方β-SiN
3Si(s)+2N(g)→SiN(s)
也可用二亚胺合成
SiCl(l)+6NH(g)→Si(NH)(s)+4NHCl(s)在0℃的条件下
3Si(NH)(s)→SiN(s)+N(g)+3H(g)在1000℃的条件下
或用碳热还原反应在1400-1450℃的氮气气氛下合成:
3SiO(s)+6C(s)+2N(g)→SiN(s)+6CO(g)
对单质硅的粉末进行渗氮处理的合成方法是在二十世纪50年代随着对氮化硅的重新“发现”而开发出来的。也是第一种用于大量生产氮化硅粉末的方法。但如果使用的硅原料纯度低会使得生产出的氮化硅含有杂质硅酸盐和铁。用二胺分解法合成的氮化硅是无定形态的,需要进一步在1400-1500℃的氮气下做退火处理才能将之转化为晶态粉末,二胺分解法在重要性方面是仅次于渗氮法的商品化生产氮化硅的方法。碳热还原反应是制造氮化硅的最简单途径也是工业上制造氮化硅粉末最符合成本效益的手段。
3SiH(g)+4NH(g)→SiN(s)+12H(g)
3SiCl(g)+4NH(g)→SiN(s)+12HCl(g)
3SiClH(g)+4NH(g)→SiN(s)+6HCl(g)+6H(g)
如果要在半导体基材上沉积氮化硅,有两种方法可供使用:
利用低压化学气相沉积技术在相对较高的温度下利用垂直或水平管式炉进行。
等离子体增强化学气相沉积技术在温度相对较低的真空条件下进行。
先利用溶胶凝胶法制备出二氧化硅,然后同时利用碳热还原法和氮化对其中包含特细碳粒子的硅胶进行处理后得到氮化硅纳米线。硅胶中的特细碳粒子是由葡萄糖在1200-1350℃分解产生的。合成过程中涉及的反应可能是:
SiO(s)+C(s)→SiO(g)+CO(g)
3SiO(g)+2N(g)+3CO(g)→SiN(s)+3CO(g)或
3SiO(g)+2N(g)+3C(s)→SiN(s)+3CO(g)
应用
材料性能
氮化硅的强度很高,尤其是热压氮化硅,是世界上最坚硬的物质之一。它极耐高温,强度一直可以维持到1200℃的高温而不下降,受热后不会熔成融体,一直到1900℃才会分解,并有惊人的耐化学腐蚀性能,能耐几乎所有的无机酸和30%以下的烧碱溶液,也能耐很多有机酸的腐蚀;同时又是一种高性能电绝缘材料。
氮化硅与水几乎不发生作用;在浓强酸溶液中缓慢水解生成铵盐和二氧化硅;易溶于氢氟酸,与稀酸不起作用。浓强碱溶液能缓慢腐蚀氮化硅,熔融的强碱能很快使氮化硅转变为硅酸盐和氨。氮化硅在600℃以上能使过渡金属(见过渡元素)氧化物、氧化铅、氧化锌和二氧化锡等还原,并放出氧化氮和二氧化氮。1285℃时氮化硅与二氮化三钙Ca3N2发生以下反应:
CaN+SiN─→3CaSiN
氮化硅的制法有以下几种:在1300~1400℃时将粉状硅与氮气反应;在1500℃时将纯硅与氨作用;
氮化硅陶瓷具有高强度、耐高温的特点,在陶瓷材料中其综合力学性能最好,耐热震性能、抗氧化性能、耐磨损性能、耐蚀性能好,是热机部件用陶瓷的第一候选材料。在机械工业,氮化硅陶瓷用作轴承滚珠、滚柱、滚球座圈、工模具、新型陶瓷刀具、泵柱塞、心轴密封材料等。
在冶金工业,由于氮化硅陶瓷耐高温,摩擦系数小,具有自润滑性。对多数金属、合金溶液稳定,因此,可制作金属材料加工的工模具,如拨轧芯棒、挤压、拨丝模具,轧辊、传送辊、发热体夹具、热偶套营、金属热处理支承件、坩埚,铝液导营、铝包内衬等。
氮化硅陶资材料在电子、军事和核工业方面也有广泛应用。
1、氮化硅陶瓷粉末的物理化性能及产品的技术指标
氮化硅陶瓷是一种白灰色粉末,分子式为:SI3N4;
分子重量:140.3,密度3.2g/cm2
其化学成分:N>38-39;0<1-1.5;C<0.1;Fe<0.2。
粒度按用户要求而定。
筛网目数与粒径(μm)对照表
目数 | 微米(μm)=10m | 目数(mesh) | 微米(μm) |
2 | 8000 | 100 | 150 |
3 | 6700 | 115 | 125 |
4 | 4750 | 120 | 120 |
5 | 4000 | 125 | 115 |
6 | 3350 | 130 | 113 |
展开表格
物理性质
相对分子质量140.28。灰色、白色或灰白色。属高温难溶化合物,无熔点,抗高温蠕变能力强,不含粘结剂的反应烧结氮化硅负荷软化点在1800℃以上;六方晶系。晶体呈六面体。反应烧结法制得的Si3N4密度为1.8~2.7g/cm3,热压法制得Si3N4密度为3.12~3.22g/cm3。莫氏硬度9~9.5,维氏硬度约为2200,显微硬度为32630MPa。熔点1900℃(加压下)。通常在常压下1900℃左右分解。比热容0.71J/(g·K)。生成热为-751.57kJ/mol。热导率为(2-155)W/(m·K)。线膨胀系数为2.8~3.2×10-6/℃(20~1000℃)。不溶于水。溶于氢氟酸。在空气中开始氧化的温度1300~1400℃。比体积电阻,20℃时为1.4×105·m,500℃时为4×108·m。弹性模量为28420~46060MPa。耐压强度为490MPa(反应烧结的)。1285℃时与二氮化二钙反应生成二氮硅化钙,600℃时使过渡金属还原,放出氮氧化物。抗弯强度为147MPa。可由硅粉在氮气中加热或卤化硅与氨反应而制得。电阻率在10^15-10^16Ω.cm。可用作高温陶瓷原料。
生产方法
其他应用
氮化硅陶瓷材料具有热稳定性高、抗氧化能力强以及产品尺寸精确度高等优良性能。由于氮化硅是键强高的共价化合物,并在空气中能形成氧化物保护膜,所以还具有良好的化学稳定性,1200℃以下不被氧化,1200~1600℃生成保护膜可防止进一步氧化,并且不被铝、铅、锡、银、黄铜、镍等很多种熔融金属或合金所浸润或腐蚀,但能被镁、镍铬合金、不锈钢等熔液所腐蚀。
氮化硅陶瓷材料可用于高温工程的部件,冶金工业等方面的高级耐火材料,化工工业中抗腐蚀部件和密封部件,机械加工工业的刀具和刃具等。
结构
氮化硅技术发展
(一)氮化硅行业技术概述
氮化硅是在人工条件下合成的化合物。虽早在140多年前就直接合成了氮化硅,但当时仅仅作为一种稳定的“难熔”的氮化物留在人们的记忆中。二次大战后,科技的迅速发展,迫切需要耐高温、高硬度、高强度、抗腐蚀的材料。经过长期的努力,直至1955年氮化硅才被重视,七十年代中期才真正制得了高质量、低成本,有广泛重要用途的氮化硅陶瓷制品。
我国自80年代中期开始研究氮化硅技术。主要是研究减重效率最高的结构氮化硅材料-多孔氮化硅材料,目前关于氮化硅复合材料的研究刚刚起步,多孔氮化硅复合材料材料组成体系的理论设计与试验设计相关研究很少,目前尚处于摸索阶段,受国内外相关研究资料较少的影响,这方面我国的研究一直处于相对落后地位,许多研究单位以及学者多把研究重点放在军工领域,而其它领域的应用研究基本尚处空白。这方面的研究有待进一步加强。多孔氮化硅陶瓷介电常数预测及其性能影响规律认识不够完全,其理论工作与试验工作的研究都很少。
(二)氮化硅制品的生产工艺:
反应烧结法生产氮化硅制品是将磨细的硅粉(粒度一般小于80μm),用机压或等静压成型,坯体干燥后,在氮气中加热至1350~1400℃,在烧成过程中同时氮化而制得。采用这种生产方法,原料条件和烧成工艺及气氛条件对制品的性能有很大的影响。
硅粉中含有许多杂质,如Fe,Ca,Aì,Ti等。Fe被认为是反应过程中的催化剂。它能促进硅的扩散,但同时,也将造成气孔等缺陷。Fe作为添加剂的主要作用:在反应过程中可作催化剂,促使制品表面生成SiO2氧化膜;形成铁硅熔系,氮溶解在液态FeSi2中,促进β-Si3N4的生成。但铁颗粒过大或含量过高,制品中也会出现气孔等缺陷,降低性能。一般铁的加入量为0~5%。Al,Ca,Ti等杂质,易与硅形成低共熔物。适当的添加量,可以促进烧结,提高制品的性能。
硅粉的粒度越细,比表面积越大,则可降低烧成温度。粒度较细的硅粉与粒度较粗的硅粉相比,制品中含α-Si3N4的量增高。降低硅粉的粒径,可以降低制品的显微气孔尺寸。适当的粒度配比,可以提高制品密度。


