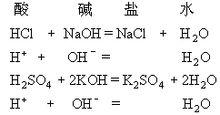离子方程式(离子符号表示离子反应的式子)

VLoG
次浏览
更新时间:2023-05-23
离子方程式
离子符号表示离子反应的式子
基本步骤
正误判断
看拆分正误
⑴能拆分的物质
如 ,错在未将
,错在未将 拆分成Ca和
拆分成Ca和 。应为:
。应为: 。
。




⑵不能拆分的物质
一、难溶物不拆
例l:向碳酸钙中加入过量盐酸。
错误:

原因: 难溶于水,像
难溶于水,像 、.AgCl、
、.AgCl、 、
、 等在书写离子方程式时均不能拆开,应写成化学式.
等在书写离子方程式时均不能拆开,应写成化学式.




正确:

二、微溶物作生成物不拆
例2:向氯化钙溶液中加入硫酸钠溶液。
错误:此反应可发生,但是 不可拆分。
不可拆分。

原因: 是微溶物,像
是微溶物,像 、
、 、
、 等微溶物,若作为生成物在书写离子方程式时均不能拆开,应写成化学式。
等微溶物,若作为生成物在书写离子方程式时均不能拆开,应写成化学式。




正确:

说明:微溶物作生成物,浓度较小时拆成离子式,浓度较大时应写成化学式。
错误:

正确:

四、氧化物不拆
错误:

原因: 是氧化物,氧化物不论是否溶于水在书写离子方程式时均不能拆开,应写成化学式。
是氧化物,氧化物不论是否溶于水在书写离子方程式时均不能拆开,应写成化学式。

正确:

错误:

原因. 是弱酸
是弱酸 的酸式酸根,像
的酸式酸根,像 ,、HS、
,、HS、 等离子在书写离子方程式时均不能拆开,应写成化学式。
等离子在书写离子方程式时均不能拆开,应写成化学式。




正确:

H与 形式,在浓溶液中不拆开,仍写成
形式,在浓溶液中不拆开,仍写成 。
。


例6:将氯化铵固体与氢氧化钙固体混合加热。
错误:

原因:写离子反应的前提是在水溶液中或熔融状态下进行的反应,固体与固体的反应尽管是离子反应,只能写化学方程式,不写离子方程式。
蔗糖、乙醇等大多数有机物是非电解质,在书写离子方程式时均不能拆开,应写分子式。
书写错误
易错分析
概述
①所有氧化物和过氧化物一律写化学式,初学者易忽略只有易溶且易电离的电解质用离子符号表示,往往将许多不可溶的强电解质拆开,导致错误。这里必须清楚,像过氧化钠、氧化钠等活泼金属氧化物或过氧化物,虽然是易溶的电解质但是不可拆。
④弱电解质、非电解质、氧化物、单质、沉淀、气体都不能拆。
32种易误拆而不能拆的物质
 | HS |  |  |  |
判断溶液中离子能否大量共存的规律
特殊多种离子能否大量共存于同一溶液中,归纳起来就是:一色,二性,三,四反应。
1.一色--溶液颜色
2.二性--溶液的酸,碱性
⑴在强酸性溶液中,OH及弱酸根阴离子(如 ,
, ,S,
,S, 等)不能大量存在。
等)不能大量存在。



⑶酸式弱酸根离子(如 ,
, HS)在强酸性或强碱性溶液中均不能大量存在。
HS)在强酸性或强碱性溶液中均不能大量存在。


3.三特殊--三种特殊情况
⑴ 与
与 不能大量共存:
不能大量共存:



4.四反应--四种反应类型
指离子间通常能发生的四种类型的反应,能相互反应的离子显然不能大量共存。
如Ba与 ,
, 与OH,H与
与OH,H与 等
等



⑵氧化还原反应
如Fe与I, 与Fe,
与Fe, 与Br等
与Br等


⑶相互促进的水解反应
如Al与
 与
与 等
等



⑷络合反应
如 与
与 等。
等。


5.看符号是否齐全
看“=” “<==>”(可逆符号)“↓” “↑”及必要条件是否正确、齐全。