诱导效应(使分子发生极化的反应)

VLoG
次浏览
更新时间:2023-05-23
诱导效应
使分子发生极化的反应

基本性质
类型
静态诱导效应:由于分子内极性共价键的存在(内在电场)而导致的,使静态分子固有的性质。对化合物反应活性的影响具有两面性,在一定条件下可增加反应活性,也可能会降低反应活性。
动态诱导效应:是发生在化学反应时,由于外界电场的出现而发生的。通常只是在进行化学反应的瞬间才表现出来,所起的作用大都是加速反应的进行。
诱导效应指数
化学活性的定量尺度。
发展简史
比较标准
诱导效应的大小和方向与原子或原子的电负性有关。在比较各种原子或原子团的诱导效应时,通常以 键中的氢原子为标准,规定
键中的氢原子为标准,规定 。
。


吸引电子能力(电负性较大)比氢原子强的原子或原子团(如 等)有吸电子的诱导效应或拉电子诱导效应(-I效应),整个分子的电子云偏向取代基。吸引电子能力比氢原子弱的原子或原子团具有给电子的诱导效应或推电子诱导效应(+I效应),整个分子的电子云偏离取代基。
等)有吸电子的诱导效应或拉电子诱导效应(-I效应),整个分子的电子云偏向取代基。吸引电子能力比氢原子弱的原子或原子团具有给电子的诱导效应或推电子诱导效应(+I效应),整个分子的电子云偏离取代基。

取代基的诱导效应强弱有如下规律:
1、同族元素中,原子序数越大,吸电子诱导效应越弱;同周期元素中,原子序数越大,吸电子诱导效应越强。
2、基团不饱和程度越大,吸电子诱导效应越强。这是由于各杂化态中s轨道成分不同而引起的,s成分越高,吸电子能力越强。
递降率
诱导效应是一种静电诱导作用,其作用随所经距离的增大而迅速减弱。诱导效应在一个σ 键体系中传递时,一般认为每经过一个链上原子,即降低为原来的约三分之一。通常以ε或1/α来表示递降率。经过n个原子后,其诱导效应只有原来的 。一般认为,经过三个原子后诱导作用可忽略。
。一般认为,经过三个原子后诱导作用可忽略。

扩展
共轭效应
共轭体系原指像 1,3-丁二烯这样单双键交替的体系,现在泛指能和 π 电子云侧面交盖并形成多原子轨道的体系。共轭体系产生共轭效应,用C 表示。若取代基使体系的 π 电子云密度增大,则该取代基具有给电子的共轭效应,用+C 表示;若取代基使体系的 π 电子云密度减小,则该取代基具有吸电子的共轭效应,用-C 表示。
共轭效应的强弱判断为:
1、原子电负性的影响。原子电负性越大,吸电子能力越强,从而给电子的共轭效应越弱。
3、取代基所带电荷的影响。负电荷越多,给电子的共轭效应越强;正电荷越多,吸电子的共轭效应
越强;通常负电荷给电子的共轭效应大于中性分子。
4、原子能级差异的影响。原子能级差异越小,共轭效应越强。
竞争关系
通过对诱导效应和共轭效应的分析,总结出便于区分二者的竞争关系,如下图:
由图可见,从左边看,结果为吸电子效应,有以下几种情况:
(1)仅有诱导效应而无共轭效应.此类取代基电负性大于碳,且母体中与取代基相连的第一个碳原子饱和。
(3)取代基为既有吸电子的共轭效应又有吸电子的诱导效应的基团( ).此类基团通常为带正电荷的基团或取代基第一个碳和非碳原子有不饱和键的基团。
).此类基团通常为带正电荷的基团或取代基第一个碳和非碳原子有不饱和键的基团。

从右边看,结果为给电子效应。
(1)仅有共轭效应而无诱导效应。这就是超共轭效应,其大小排列顺序为:

(3)取代基为能产生 共轭的某些复杂基团此类取代基大多比较复杂,基团中一般包含有孤对电子的原子以及碳碳不饱和键,形成
共轭的某些复杂基团此类取代基大多比较复杂,基团中一般包含有孤对电子的原子以及碳碳不饱和键,形成  共轭。既可能是吸电子效应也可能是给电子效应.通常为某些二价共轭体系基团。
共轭。既可能是吸电子效应也可能是给电子效应.通常为某些二价共轭体系基团。


应用
一般来说:
1、体系越缺电子,酸性越强;体系越富电子,碱性越强。
3、越稳定的物质越容易生成.反应过程中,稳定中间体的生成量最多,反应速率也最快,有些物质可能会通过重排生成更稳定的中间体;反应的最终产物以最稳定的物质为主。
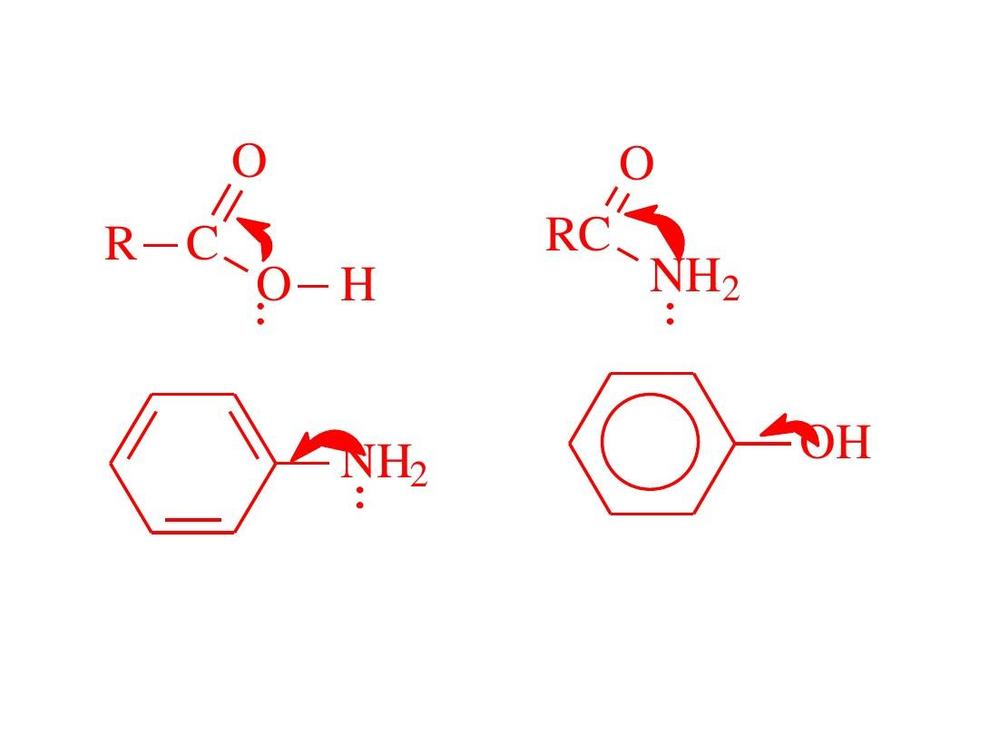
举例:比较下列化合物的酸性并排序。
答案:

解析:芳环羧酸的邻位异构体的酸性是最强的,原因为:
(2)共轭效应。间位和对位的诱导效应很弱,以共轭效应为主,且间位共轭效应大于对位。共轭效应使得羰基上的电子云密度增大,对羧基的吸引力减小,故而使得所示的酸性解离减弱。