生物氧化(物质在生物体内发生氧化的过程)

VLoG
次浏览
更新时间:2023-05-19
生物氧化
物质在生物体内发生氧化的过程
基本信息
| 部位 | 线粒体 、细胞膜 |
| 特点 | 为机体提供可利用的能量 |
| 过程 | 酶促反应与氧化合成水 |
基本概况
(1)是在细胞内进行酶催化的氧化过程,反应条件温和(水溶液中PH约为7和常温)。
(2)在生物氧化的过程中,同时伴随生物还原反应的产生。
(4)在生物氧化中,碳的氧化和氢化是非同步进行的。氧化过程中脱下来的质子和电子,通常由各种载体,如NADH等传递给氧并最终生成水。
(5)生物氧化是一个分步进行的过程。每一步都有特殊的酶催化,每一步反应的产物都可以分离出来。这种逐步反应的模式有利于在温和的条件下释放能量,提高能源利用率。
(6)生物氧化释放的能量,通过与ATP合成相偶联,转换成生物体能够直接利用的生物能ATP。
氧化生成
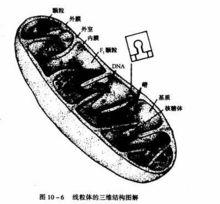
生物氧化
中水的生成
代谢物上的氢原子被脱氢酶激活脱落后,经过一系列的传递体,最后与激活的氧结合生成水的全部体系,此过程与细胞呼吸有关,所以将此传递链称为呼吸链(respiratory chain)或电子传递链(electron transfer chain)。
生物体内的呼吸链有多种型式。人体细胞线粒体内最重要的有两条,即NADH氧化呼吸链和琥珀酸氧化呼吸链。它们的初始受氢体、生成ATP的数量及应用有差别。NADH氧化呼吸链应用最广,糖、脂、蛋白质三大物质分解代谢中的脱氢氧化反应,绝大多数是通过该呼吸链来完成的。琥珀酸氧化呼吸链在Q处与上述NADH氧化呼吸链途径交汇。其脱氢黄酶只能催化某些代谢物脱氢,不能催化NADH或NADPH脱氢。
(二)呼吸链的组成
组成呼吸链的成分已发现20余种,分为5大类。
1.辅酶Ⅰ和辅酶Ⅱ
辅酶Ⅰ(NAD+或CoⅠ)为烟酰胺腺嘌呤二核苷酸。辅酶Ⅱ(NADP+或CoⅡ)为烟酰胺腺嘌呤二核苷酸磷酸。它们是不需氧脱氢酶的辅酶,分子中的烟酰胺部分,即维生素PP能可逆地加氢还原或脱氢氧化,是递氢体。以NAD+作为辅酶的脱氢酶占多数。
2.黄素酶
黄素酶的种类很多,辅基有2种,即FMN和FAD。FMN是NADH脱氢酶的辅基,FAD是琥珀酸脱氢酶的辅基,都是以核黄素为中心构成的,其异咯嗪环上的第1位及第5位两个氮原子能可逆地进行加氢和脱氢反应,为递氢体。
3.铁硫蛋白
分子中含有非血红素铁和对酸不稳定的硫,因而常简写为FeS形式。在线粒体内膜上,常与其他递氢体或递电子体构成复合物,复合物中的铁硫蛋白是传递电子的反应中心,亦称铁硫中心,与蛋白质的结合是通过Fe与4个半胱氨酸的S相连接。
4.泛醌(又名辅酶Q)
5.细胞色素类
Cyta和a3 结合紧,迄今尚未分开,故写成aa3,位于呼吸链的终末部位,其辅基为血红素A,传递电子的机制是以辅基中铁价的变化Fe3+ →Fe2+,a3还含有铜离子,把电子直接交给分子氧Cu+ →Cu2+,所以a3又称细胞色素氧化酶。a3中的铁原子可以与氧结合,也可以与氰化物离子(CN—)、CO等结合,这种结合一旦发生,a3便失去使氧还原的能力,电子传递中止,呼吸链阻断,导致机体不能利用氧而窒息死亡。
(三)呼吸链中传递体的顺序
呼吸链中氢和电子的传递有着严格的顺序和方向。根据氧化还原原理,氧化-还原电势E是物质对电子亲和力的量度,电极电位的高低反映电子得失的倾向,E O'值愈低的氧还对(A/AH2)释放电子的倾向愈大,愈容易成为还原剂而排在呼吸链的前面。所以NADH还原能力最强,氧分子的氧化能力最强。电子的自发流向是从电极电位低的物质(还原态)到电位高的氧化态,目前一致认可的是按标准氧还电位递增值依次排列。
氧化磷酸化
偶联部位
2.偶联部位:根据实验测定氧的消耗量与ATP的生成数之间的关系以及计算氧化还原反应中ΔGO'和电极电位差ΔE的关系可以证明。
P/O比值是指代谢物氧化时每消耗1摩尔氧原子所消耗的无机磷原子的摩尔数,即合成ATP的摩尔数。实验表明, NADH在呼吸链被氧化为水时的P/O值约等于3,即生成3分子ATP?(1~6版生物化学此数据为3,7版为2.5);FADH2氧化的P/O值约等于2,即生成2分子ATP(1~6版生物化学此数据为2,7版为1.5)。
氧-还电势沿呼吸链的变化是每一步自由能变化的量度。根据ΔGO'= - nFΔE O'(n是电子传递数,F是法拉第常数),从NADH到Q段电位差约0.36V,从Q到Cytc为0.21V,从aa3到分子氧为0.53V,计算出相应的ΔGO'分别为69.5、40.5、102.3kJ/mol。于是普遍认为下述3个部位就是电子传递链中产生ATP的部位。
NADH→NADH脱氢酶→‖Q → 细胞色素bc1复合体→‖Cytc →aa3→‖O2
氧化作用
糖代谢中的三羧酸循环和脂肪酸β-氧化是在线粒体内生成NADH(还原当量),可立即通过电子传递链进行氧化磷酸化。在细胞的胞浆中产生的NADH ,如糖酵解生成的NADH则要通过穿梭系统(shuttle system)使NADH的氢进入线粒体内膜氧化。
(一)α-磷酸甘油穿梭作用
胞液中的NADH在α-磷酸甘油脱氢酶的催化下,使磷酸二羟丙酮还原为α-磷酸甘油,后者通过线粒体内膜,并被内膜上的α-磷酸甘油脱氢酶(以FAD为辅基)催化重新生成磷酸二羟丙酮和FADH2,后者进入琥珀酸氧化呼吸链,生成1.5分子ATP。葡萄糖在这些组织中彻底氧化生成的ATP比其他组织要少,1摩尔G→30摩尔ATP。
(二)苹果酸-天冬氨酸穿梭作用
主要存在肝和心肌中。1摩尔G→32摩尔ATP
偶联机制
1961年,英国学者Peter Mitchell提出化学渗透假说(1978年获诺贝尔化学奖),说明了电子传递释出的能量用于形成一种跨线粒体内膜的质子梯度(H+梯度),这种梯度驱动ATP的合成。这一过程概括如下:
2.H+ 泵出,在膜间隙产生一高的H+ 浓度,这不仅使膜外侧的pH较内侧低(形成pH梯度),而且使原有的外正内负的跨膜电位增高,由此形成的电化学质子梯度成为质子动力,是H+ 的化学梯度和膜电势的总和。
3.H+ 通过ATP合酶流回到线粒体基质,质子动力驱动ATP合酶合成ATP。
(二)ATP合酶
ATP合酶由两部分组成(Fo-F1),球状的头部F1突向基质液,水溶性。亚单位Fo埋在内膜的底部,是疏水性蛋白,构成H+ 通道。在生理条件下,H+ 只能从膜外侧流向基质,通道的开关受柄部某种蛋白质的调节。
相关因素
(一)抑制剂
能阻断呼吸链某一部位电子传递的物质称为呼吸链抑制剂。
抗霉素A抑制电子在细胞色素bc1复合体处的传递。
氰化物、CO、叠氮化物(N3-)抑制细胞色素氧化酶。
(二)解偶联剂
2,4-二硝基苯酚(DNP)和颉氨霉素可解除氧化和磷酸化的偶联过程,使电子传递照常进行而不生成ATP。DNP的作用机制是作为H+的载体将其运回线粒体内部,破坏质子梯度的形成。由电子传递产生的能量以热被释出。
(三)ADP的调节作用
正常机体氧化磷酸化的速率主要受ADP水平的调节,只有ADP被磷酸化形成ATP,电子才通过呼吸链流向氧。如果提供ADP,随着ADP的浓度下降,电子传递进行,ATP在合成,但电子传递随ADP浓度的下降而减缓。此过程称为呼吸控制,这保证电子流只在需要ATP合成时发生。


