蛋白质代谢(蛋白质在细胞内的代谢途径)

VLoG
次浏览
更新时间:2023-05-23
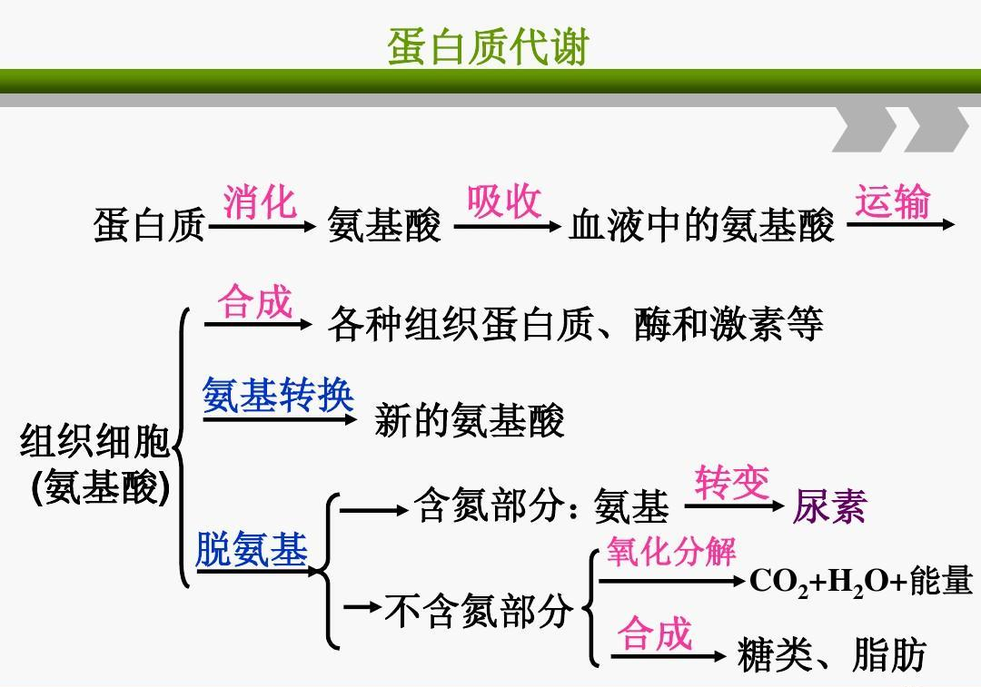
蛋白质代谢
蛋白质在细胞内的代谢途径
基本信息
| 中文名 | 蛋白质代谢 |
| 外文名 | protein metabolism |
| 拼音 | dàn bái zhì dài xiè |
| 定义 | 蛋白质 在细胞内的代谢途径 |
| 类别 | 混合物 |
实现途径
1、蛋白质代谢以氨基酸为核心,细胞内外液中所有游离氨基酸称为游离氨基酸库,其含量不足氨基酸总量的1%,却可反映机体氮代谢的概况。食物中的蛋白都要降解为氨基酸才能被机体利用,体内蛋白也要先分解为氨基酸才能继续氧化分解或转化。
2、游离氨基酸可合成自身蛋白,可氧化分解放出能量,可转化为糖类或脂类,也可合成其他生物活性物质。合成蛋白是主要用途,约占75%,而蛋白质提供的能量约占人体所需总能量的10-15%。蛋白质的代谢平衡称氮平衡,一般每天排出5克氮,相当于30克蛋白质。
合成代谢
多肽合成
1.转录
在转录中,RNA聚合酶读取DNA链并产生可以进一步翻译的mRNA链。为了启动转录,要转录的DNA片段必须是可接近的(即它不能紧密包装)。一旦DNA片段可及,RNA聚合酶就可以通过将RNA核苷酸与模板DNA链配对来开始转录编码DNA链。在初始转录阶段期间,RNA聚合酶在DNA模板链上搜索启动子区域。一旦RNA聚合酶与该区域结合,它就开始以3'至5'方向“读取”模板DNA链。RNA聚合酶附着与模板DNA链互补的RNA碱基(将使用尿嘧啶代替胸腺嘧啶)。新的核苷酸碱基共价键合。新碱基最终与DNA碱基分离,但保持相互连接,形成新的mRNA链。该mRNA链以5'至3'方向合成。一旦RNA到达终止子序列,它就会从DNA模板链解离并终止mRNA序列。
通过转录因子在细胞中调节转录。转录因子是与DNA链中的调节序列结合的蛋白质,例如启动子区域或操纵子区域。与这些区域结合的蛋白质可以直接停止或允许RNA聚合酶读取DNA链,或者可以指示其他蛋白质停止或允许RNA聚合酶读取。
2.翻译
在翻译过程中,核糖体将mRNA序列(信使RNA)转化为氨基酸序列。每个3碱基对长的mRNA区段是对应于一个氨基酸或终止信号的密码子。氨基酸可以具有与其对应的多个密码子。核糖体不直接将氨基酸连接至mRNA密码子。他们也必须利用tRNA(转移RNA)。转移RNA可以与氨基酸结合并含有可与氢结合mRNA密码子的反密码子。将氨基酸与tRNA结合的过程称为tRNA充电。这里,氨基酰基-tRNA合成酶催化两个反应。在第一个中,它将AMP分子(从ATP切割)附着到氨基酸上。第二反应裂解氨酰基-AMP产生能量以将氨基酸连接至tRNA分子。
核糖体有两个亚基,一个大,一个小。这些亚基围绕mRNA链。较大的亚基含有三个结合位点:A(氨基酰基),P(肽基)和E(出口)。在翻译起始后(其在原核生物和真核生物中不同),核糖体进入延长期,其遵循重复循环。首先,具有正确氨基酸的tRNA进入A位点。核糖体将肽从P位点的tRNA转移到A位点的tRNA上的新氨基酸。来自P位点的tRNA将被转移到E位点,在那里它将被弹出。这种情况持续发生,直到核糖体到达终止密码子或接收到停止的信号。A.肽键与P位点中与tRNA连接的氨基酸和与A位点中的tRNA连接的氨基酸形成。肽键的形成需要能量输入。两个反应分子是一个氨基酸的α氨基和另一个氨基酸的α羧基。这种键形成的副产物是水的释放(氨基提供质子,而羧基提供羟基)。
翻译可以下调的miRNA的(微RNA)。这些RNA链可以切割它们互补的mRNA链,从而停止翻译。翻译也可以通过辅助蛋白进行调节。例如,称为真核起始因子-2(eIF-2)的蛋白质可以与核糖体的较小亚基结合,开始翻译。当elF-2被磷酸化时,它不能与核糖体结合并停止翻译。
3.翻译后修饰
一旦肽链合成,它仍然必须被修饰。翻译后修饰可以在蛋白质折叠之前或之后发生。翻译后修饰肽链的常见生物学方法包括甲基化,磷酸化和二硫键形成。甲基化通常发生于精氨酸或赖氨酸和涉及将甲基的氮(置换氢)。这些氨基酸上的R基团可以被甲基化只要与氮的键不超过4,就会多次。甲基化降低了这些氨基酸形成氢键的能力,因此甲基化的精氨酸和赖氨酸具有与其标准对应物不同的性质。磷酸化通常发生在丝氨酸,苏氨酸和酪氨酸上,并涉及用磷酸基团取代R基团末端的醇基上的氢。这增加了R基团的负电荷,因此将改变氨基酸与其标准对应物相比的行为方式。二硫键形成是二硫键(共价键)的产生)在链中的两个半胱氨酸氨基酸之间,其增加了折叠结构的稳定性。
肽链的盘曲折叠
4.蛋白质折叠
细胞中的多肽链不必保持线性;它可以变成分支或折叠在自身上。多肽链以特定方式折叠,这取决于它们所处的溶液。所有氨基酸含有具有不同性质的R基团的事实是蛋白质折叠的主要原因。在诸如胞质溶胶的亲水环境中,疏水性氨基酸将集中在蛋白质的核心,而亲水性氨基酸将在外部。这是熵有利的因为水分子可以比疏水性氨基酸更自由地在亲水性氨基酸周围移动。在疏水环境中,亲水性氨基酸将集中在蛋白质的核心,而疏水性氨基酸将在外部。由于亲水性氨基酸之间的相互作用强于疏水性-亲水性相互作用,因此这在焓方面是有利的。一旦多肽链完全折叠,它就被称为蛋白质。尽管存在仅含有一条多肽链的生理蛋白,但通常许多亚基将组合形成功能完整的蛋白质。蛋白质还可以结合其他分子,如血红素基团中的血红蛋白,一种负责携带血液中氧气的蛋白质。
分解代谢
酶的蛋白质
1.蛋白酶
最初被认为仅破坏酶促反应,蛋白酶(也称为肽酶)实际上通过切割帮助分解代谢蛋白质并产生之前不存在的新蛋白质。蛋白酶也有助于调节代谢途径。他们这样做的一种方法是在不需要运行的途径中切割酶(即当血糖浓度高时糖原异生)。这有助于节省尽可能多的能量并避免徒劳无功的循环。当分解代谢和合成代谢途径在相同时间和相同反应的速率下都有效时,发生无效循环。由于产生的中间体被消耗,因此身体不会产生净增益。能量通过徒劳的循环而消失。蛋白酶通过改变其中一种途径的速率来阻止这种循环,或者通过切割关键酶,它们可以阻止其中一种途径。当与底物结合时,蛋白酶也是非特异性的,允许细胞和其他蛋白质内的大量多样性,因为它们可以以能量有效的方式更容易地裂解。
因为许多蛋白酶是非特异性的,它们在细胞中受到高度调节。没有调节,蛋白酶会破坏生理过程中的许多必需蛋白质。身体调节蛋白酶的一种方法是通过蛋白酶抑制剂。蛋白酶抑制剂可以是其他蛋白质,小肽或分子。有两种类型的蛋白酶抑制剂:可逆和不可逆。可逆蛋白酶抑制剂与限制其功能的蛋白酶形成非共价相互作用。它们可以是竞争性抑制剂,非竞争性抑制剂和非竞争性抑制剂。竞争性抑制剂与肽竞争结合蛋白酶活性位点。当竞争肽结合时,非竞争性抑制剂与蛋白酶结合,但不让蛋白酶切割肽键。非竞争性抑制剂可以做到这两点。不可逆的蛋白酶抑制剂共价修饰蛋白酶的活性位点,因此它不能切割肽。
2.外肽酶
外肽酶是主要通过添加水来切割氨基酸侧链末端的酶。这些酶有两类:氨肽酶和羧肽酶。氨肽酶是从蛋白质的氨基末端去除氨基酸的酶。它们存在于所有生命形式中并且对于生存至关重要,因为它们为了保持稳定而执行许多细胞任务。这种形式的肽酶是锌金属酶,它被过渡态类似物抑制。该模拟类似于实际的过渡状态因此它可以使酶与其结合而不是实际的过渡态,从而防止底物结合并降低反应速率。羧肽酶在蛋白质的羧基末端裂解。虽然它们可以使蛋白质分解代谢,但它们更常用于转录后修饰。
3.内肽酶
环境变化
1.pH
细胞蛋白质保持在相对恒定的pH中,以防止氨基酸质子化状态的变化。如果pH下降,如果其R基团的pka高于新的pH,则多肽链中的一些氨基酸可以质子化。质子化可以改变这些R基团的电荷。如果pH升高,链中的一些氨基酸可以去质子化(如果R基团的pka低于新的pH)。这也改变了R组的费用。由于许多氨基酸基于静电吸引力与其他氨基酸相互作用,改变电荷可以打破这些相互作用。这些相互作用的丧失改变了蛋白质结构,但最重要的是它改变了蛋白质功能,这可能是有益的或有害的。pH的显着变化甚至可以破坏氨基酸产生的许多相互作用并使蛋白质变性(展开)。
2.温度
随着环境温度的升高,分子移动得更快。氢键和疏水相互作用是蛋白质中重要的稳定力。如果温度升高并且含有这些相互作用的分子移动得太快,则相互作用会受到损害甚至破坏。在高温下,不能形成这些相互作用,并且功能性蛋白质变性。但是,它依赖于两个因素;使用的蛋白质类型和施加的热量。施加的热量决定了蛋白质的这种变化是永久性的还是可以转变回其原始形式。
消化过程
外源蛋白有抗原性,需降解为氨基酸才能被吸收利用。只有婴儿可直接吸收乳汁中的抗体。可分为以下两步:
降解蛋白


